Перейти к:
Обоснование гигиенического норматива содержания в воздухе рабочей зоны фармацевтической субстанции клиндамицина гидрохлорида с учётом его токсических свойств, подтверждённых в хроническом ингаляционном эксперименте
https://doi.org/10.47470/0869-7922-2025-33-6-493-501
EDN: qujovi
Аннотация
Введение. Расширение производства антибактериальных лекарственных средств, в том числе клиндамицина гидрохлорида (КГ), и контакта с ними работников определили актуальность экспериментальных исследований по обоснованию предельно допустимой концентрации КГ в воздухе рабочей зоны (ПДКврз).
Материал и методы. С использованием физиологических, поведенческих, гематологических, биохимических и гистологических методов изучена выраженность токсических проявлений у белых крыс, получавших ингаляционно в течение четырёх месяцев три последовательно трёхкратно снижающиеся концентрации КГ.
Результаты. Хроническое ингаляционное воздействие на животных КГ в концентрации 13,5 мг/м³ привело к значимым сдвигам гематологических (увеличение количества лейкоцитов за счёт значительного возрастания количества моноцитов) и биохимических показателей сыворотки крови (повышение уровней мочевины, общего билирубина и снижение концентрации прямого билирубина и холестерина), выраженным патоморфологическим изменениям в лёгочной ткани, печени, почках, миокарде и селезёнке. Воздействие на крыс КГ в концентрации 4,4 мг/м³ сопровождалось менее выраженными и распространёнными токсическими эффектами (повышение общего билирубина и снижение уровней прямого билирубина и холестерина в сыворотке крови, преимущественно слабые структурные изменения в бронхах, лёгочной паренхиме и селезёнке). У опытных животных после хронического воздействия КГ в концентрации 1,6 мг/м³ все изученные морфофункциональные показатели и гистологические характеристики внутренних органов не имели существенных отличий от контрольных.
Ограничения исследования. Исследования ограничены изучением токсического действия фармацевтической субстанции КГ в хроническом эксперименте при ингаляционном воздействии. Результаты исследования применимы для обоснования предельно допустимой концентрации исследуемой субстанции в воздухе рабочей зоны (ПДКврз).
Заключение. На основании результатов ингаляционного эксперимента в качестве пороговой хронического токсического действия принята концентрация КГ 4,4 мг/м³ – более чем в три раза ниже ранее установленных величин пороговых концентраций субхронического специфического дисбиотического и аллергического действий. Это определило ведущее вредное общетоксическое действие на организм как критерий гигиенического нормирования КГ. С учётом рассчитанного коэффициента запаса (11) к пороговой концентрации хронического токсического действия обоснована ПДКврз аэрозоля клиндамицина гидрохлорида на уровне 0,4 мг/м³ (II класс опасности).
Соблюдение этических стандартов. Исследования выполнены в соответствии с принципами Европейской конвенции по защите позвоночных животных, используемых для экспериментальных и иных научных целей (Страсбург, 18 марта 1986 г.), директивы Европейского парламента и Европейского Союза по охране животных, используемых в экспериментах 2010/63/EU, и одобрены Комиссией по биоэтике Республиканского унитарного предприятия «Научно-практический центр гигиены» от 29.03.2022 г. № 2.
Участие авторов:
Земцова В.О. – сбор и обработка материала, статистический анализ, написание текста;
Богданов Р.В. – концепция и дизайн исследования, редактирование;
Рябцева С.Н. – сбор и обработка материала, статистический анализ;
Шевляков В.В. – написание текста, редактирование;
Сычик С.И. – концепция и дизайн исследования, редактирование;
Чернышова Е.В. – сбор и обработка материала.
Все соавторы – утверждение окончательного варианта статьи, ответственность за целостность всех её частей.
Конфликт интересов. Авторы заявляют об отсутствии явных и потенциальных конфликтов интересов в связи с публикацией данной статьи.
Финансирование. Работа проведена в рамках выполнения задания 03.10 ГНТП «Научно-техническое обеспечение качества и доступности медицинских услуг» на 2021–2025 гг. и финансирована из средств республиканского бюджета.
Поступила в редакцию: 19 марта 2025 / Поступила после исправления: 06 июня 2025 / Принята в печать: 25 ноября 2025 / Опубликована: 15 января 2026
Ключевые слова
Для цитирования:
Земцова В.О., Богданов Р.В., Рябцева С.Н., Шевляков В.В., Сычик С.И., Чернышова Е.В. Обоснование гигиенического норматива содержания в воздухе рабочей зоны фармацевтической субстанции клиндамицина гидрохлорида с учётом его токсических свойств, подтверждённых в хроническом ингаляционном эксперименте. Токсикологический вестник. 2025;33(6):493-501. https://doi.org/10.47470/0869-7922-2025-33-6-493-501. EDN: qujovi
For citation:
Zemtsova V.O., Bogdanov R.V., Rjabceva S.N., Shevlyakov V.V., Sychik S.I., Chernyshova E.V. Justification of the hygienic standard for the content of the pharmaceutical substance clindamycin hydrochloride in the air of the working area, taking into account its toxic properties, confirmed in a chronic inhalation experiment. Toxicological Review. 2025;33(6):493-501. (In Russ.) https://doi.org/10.47470/0869-7922-2025-33-6-493-501. EDN: qujovi
Введение
Антибактериальные лекарственные средства составляют значительную часть номенклатуры производимой фармацевтической продукции и широко применяются в медицине и ветеринарии. Рост объёмов их промышленного производства сопровождается увеличением числа работников, подвергающихся профессиональному воздействию, что обусловливает необходимость комплексной оценки рисков для здоровья работающих и разработки гигиенических нормативов и методов контроля содержания антибактериальных лекарственных средств в воздухе рабочей зоны [1–4].
В общем объёме производимых в Республике Беларусь антибактериальных лекарственных средств значительную долю составляет клиндамицина гидрохлорид (КГ) – полусинтетический антибиотик группы линкозамидов, обладающий высокой терапевтической значимостью и применяемый для лечения инфекционно-воспалительных болезней, вызванных чувствительными к нему штаммами микроорганизмов [5–6].
Цель работы – изучение в хроническом эксперименте при ингаляционном воздействии токсического действия фармацевтической субстанции КГ и обоснование её предельно допустимой концентрации в воздухе рабочей зоны (ПДКврз).
Материал и методы
Токсическое действие фармацевтической субстанции КГ изучали в снижающихся концентрациях в условиях хронического ингаляционного воздействия на нелинейных белых крыс [7]. До эксперимента животные находились в карантине в течение 14 дней в условиях вивария. Группы (три экспериментальных и одна контрольная, по 10 крыс в каждой) формировали методом случайной выборки, разность в массе животных составила не более 10% [7, 8].
Схема эксперимента предполагала ежедневное (5 дней в неделю) ингаляционное поступление КГ в течение четырёх месяцев в следующих концентрациях: первая опытная группа животных – 13,5 мг/м³, вторая – 4,4 мг/м³, третья – 1,6 мг/м³. Выбор концентраций обоснован результатами изучения специфического действия КГ в субхронических ингаляционных экспериментах [9–13].
Для оценки токсического действия КГ на основные органы и системы определяли массу тела животных, относительные коэффициенты массы внутренних органов (ОКМ), суммационно-пороговый показатель (СПП), двигательную активность с использованием теста «открытое поле». После завершения эксперимента белых крыс выводили из опыта методом мгновенной декапитации, проводили макроскопическое и гистологическое исследование внутренних органов для выявления морфологических признаков токсического действия и определения органов-мишеней, исследовали показатели периферической крови, биохимические параметры сыворотки крови и функциональное состояние мочевыделительной системы. В процессе микроскопического исследования анализировали наличие или отсутствие патологических процессов в гистологических срезах органов крыс. Воспалительную инфильтрацию оценивали полуколичественным способом с указанием степени её выраженности: слабая, умеренная и выраженная.
Манипуляции с лабораторными животными проводили в соответствии с принципами Европейской конвенции по защите позвоночных животных, используемых для экспериментальных и иных научных целей (Страсбург, 18 марта 1986 г.), директивы Европейского парламента и Европейского Союза по охране животных, используемых в экспериментах 2010/63/EU, и на основании разрешения, выданного комиссией по биоэтике Республиканского унитарного предприятия «Научно-практический центр гигиены» от 29.03.2022 г. № 2.
Экспериментальные данные обрабатывались с использованием лицензионного программного обеспечения Statistica 10. Значимость наблюдаемых различий двух независимых групп оценивали с помощью непараметрического критерия Манна – Уитни (Mann–Whitney U-test). Данные представлены в виде медианы (Ме), 25-го и 75-го процентилей, различия считались статистически значимыми при p < 0,05. Выявленные качественные микроскопические изменения органов представлены в относительных значениях (%), количественные – в виде медианы (Ме), 25-го и 75-го процентилей.
Результаты
По результатам исследования токсического действия КГ после завершения четырёхмесячного хронического ингаляционного эксперимента установлено, что величины изученных физиологических (масса тела, СПП) и этологических показателей индивидуального поведения белых крыс всех трёх опытных групп не имели существенных различий с таковыми в контрольной группе. При этом лишь воздействие максимальной изученной концентрации вызывало у животных первой опытной группы увеличение абсолютной и относительной массы печени (р < 0,05) при отсутствии статистически значимых различий величин ОКМ других внутренних органов по сравнению с таковыми у крыс контрольной группы.
Со стороны изученных гематологических показателей также только у животных первой опытной группы установлено увеличение количества лейкоцитов на 16% (р < 0,05), в основном за счёт значительного увеличения количества моноцитов – на 34,5% (р < 0,01) по сравнению с контрольной группой.
При анализе биохимических показателей сыворотки крови у животных опытных групп выявлен ряд статистически значимых изменений. Так, воздействие КГ в максимальной изученной концентрации вызывало увеличение в сыворотке крови крыс первой опытной группы содержания мочевины на 50,5% по сравнению с контрольной группой (с 4,12 мМоль/л до 6,20 мМоль/л), что указывает на возможные нарушения функции почек и усиление протеолиза белка.
Одним из ключевых биохимическим маркёров функционального состояния печени является билирубин, который участвует в метаболизме гемсодержащих белков. Установлено увеличение содержания в сыворотке крови животных первой опытной группы общего билирубина в 3,7 раза (р < 0,05), а у крыс второй опытной группы – на 80,1% (р < 0,05) по сравнению с контролем. Повышение уровня билирубина свидетельствует о возможном гемолизе эритроцитов и нарушении функций печени, что подтверждается литературными данными о гепатотоксичности линкозамидов [14]. В то же время отмечено снижение в сыворотке крови опытных животных первой и второй групп уровня прямого билирубина соответственно на 67,3% (р < 0,05, с 0,52 мкмоль/л до 0,17 мкмоль/л) и 61,5% (р < 0,05, с 0,52 мкмоль/л до 0,20 мкмоль/л) по сравнению с контролем, что может указывать на дисфункцию гепатоцитов и нарушение конъюгации билирубина в печени.
О нарушении липидного обмена в организме экспериментальных животных после воздействия КГ в концентрации 13,5 мг/м³ свидетельствует снижение в сыворотке крови уровня холестерина на 21,4% (р < 0,05), что, возможно, обусловлено токсическим действием препарата на метаболизм желчных кислот в печени.
Не выявлено существенного влияния КГ в испытанных концентрациях на функциональное состояние мочевыводящей системы животных, поскольку не установлены достоверные изменения изученных показателей мочи животных всех опытных групп по сравнению с контролем.
При этом длительное ингаляционное воздействие КГ в наименьшей изученной концентрации на уровне 1,6 мг/м³ не вызывало у крыс третьей опытной группы статистически значимых изменений всех изученных морфофункциональных показателей по сравнению с контрольной группой.
По завершении эксперимента выполнены патоморфологические исследования внутренних органов крыс контрольной и опытных групп. У крыс первой опытной группы наблюдались изменения гистоморфологической картины сердца, свидетельствовавшие о нарушении клеточного метаболизма: отчётливая дистрофия кардиомиоцитов, проявляющаяся неоднородностью цитоплазматического окрашивания, локальными участками гиперхромии и гипохромии ядер. У 40% животных выявлены участки контрактурных изменений мышечных волокон, что указывало на развитие ишемически-дистрофических процессов в миокарде.
У животных второй опытной группы подобные патологические изменения наблюдались в минимальной степени, а у крыс третьей опытной группы гистологическая характеристика сердца была аналогична таковой у контрольных животных.
В лёгочной паренхиме и бронхах крыс первой опытной группы выявлена выраженная гиперплазия бокаловидных клеток, сопровождаемая значительным снижением числа функционирующих реснитчатых клеток, что может приводить к нарушению мукоцилиарного клиренса (рис. 1, а, см. на вклейке).
При этом в подслизистой основе трахеи и бронхов отмечены признаки воспалительной инфильтрации, преимущественно лимфоцитарно-макрофагального характера, а в лёгочной паренхиме – периваскулярная и перибронхиальная инфильтрация, утолщение межальвеолярных перегородок (рис. 2, а, см. на вклейке).
У белых крыс второй опытной группы в лёгких определены менее выраженные изменения, характеризующиеся умеренной инфильтрацией подслизистого слоя бронхов и незначительной гиперплазией бокаловидных клеток, минимальным утолщением межальвеолярных перегородок лёгочной паренхимы (рис. 2, б, см. на вклейке).
Морфологическое исследование почечной ткани экспериментальных животных выявило дозозависимые патологические изменения, затрагивающие как клубочковый, так и канальцевый аппараты. Так, в почках животных первой опытной группы отмечено выраженное утолщение базальной мембраны капилляров клубочков (рис. 3, а, б, см. на вклейке), сопровождаемое признаками дистрофии эпителия проксимальных извитых канальцев: вакуолизация цитоплазмы, деструкция апикального полюса клеток и наличие гиалиновых капель в просвете канальцев. Эти изменения свидетельствуют об усиленной экскреции белков и нарушении процессов реабсорбции.
У животных, подвергшихся воздействию КГ в концентрации 4,4 мг/м³, выявлены менее выраженные изменения в почках: очаговая зернистая дистрофия эпителия проксимальных канальцев, умеренная вакуолизация цитоплазмы и незначительное утолщение базальной мембраны клубочков.
Воздействие максимально изученной концентрации 13,5 мг/м³ вызывало у опытных крыс гиалиново-капельную и (или) мелкокапельную жировую дистрофию гепатоцитов, а также признаки разобщённого окисления, характеризующиеся неравномерной вакуолизацией цитоплазмы (рис. 4, а, б, в, см. на вклейке). Воспалительная инфильтрация в портальных трактах выявлена у 80% животных, а у 20% отмечены признаки начального фиброза. В печени белых крыс второй опытной группы наблюдались лишь единичные дистрофические изменения.
У животных первой опытной группы выявлена значительная морфологическая перестройка лимфоидной ткани селезёнки (гипоплазия отдельных лимфофолликулов и гиперплазия других), что свидетельствовало о напряжении иммунного ответа. Красная пульпа селезёнки характеризовалась полнокровием синусоидов и снижением клеточной плотности. У белых крыс второй опытной группы изменения в селезёнке были менее выражены и ограничивались очаговой гиперплазией маргинальной зоны лимфоидных фолликулов белой пульпы.
У животных третьей опытной группы после хронического ингаляционного воздействия КГ в концентрации 1,6 мг/м³ каких-либо патологических изменений внутренних органов не установлено.
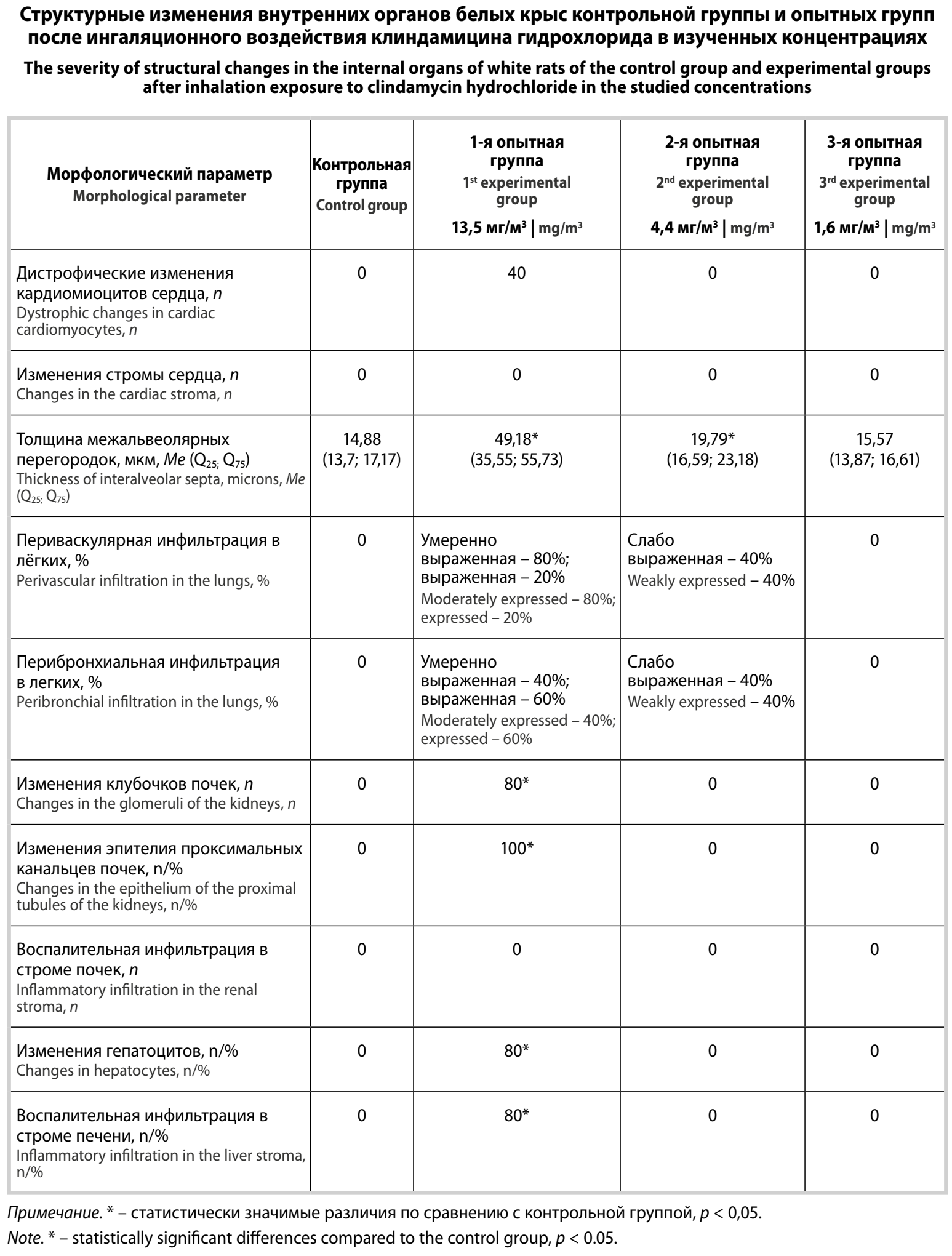
В таблице приведены обобщённые количественные характеристики структурных изменений внутренних органов белых крыс контрольной и опытных групп. Установлены достоверные различия толщины межальвеолярных перегородок лёгких крыс после ингаляционного воздействия КГ в концентрациях 13,5 мг/м³ (р < 0,0001) и 4,4 мг/м³ (р < 0,001) по сравнению с аналогичными значениями у крыс контрольной группы. Также выявлены статистически значимые различия между животными контрольной и первой опытной групп по следующим морфологическим параметрам: периваскулярная инфильтрация в лёгких (р = 0,0122), перибронхиальная инфильтрация в лёгких (р = 0,0122), изменения клубочков почек (р = 0,0472), изменения эпителия проксимальных канальцев почек (р = 0,0122), дистрофические изменения гепатоцитов (р = 0,0472) и воспалительная инфильтрация в строме печени (р = 0,0122).
Обсуждение
Выполненными экспериментальными исследованиями установлен характер и выраженность дозозависимого токсического действия на белых крыс фармацевтической субстанции клиндамицина гидрохлорида при хроническом четырёхмесячном ингаляционном поступлении в снижающихся концентрациях.
- В испытанной концентрации на уровне 13,5 мг/м³ препарат оказывал выраженное токсическое действие на организм белых крыс, выраженное в достоверном возрастании массы печени, значимых сдвигах ряда гематологических (увеличение количества лейкоцитов за счёт значительного возрастания количества моноцитов) и биохимических показателей сыворотки крови (повышение уровней мочевины, общего билирубина и снижение концентрации прямого билирубина и холестерина), развитии очевидных патологических изменений в лёгочной ткани (признаки интерстициального пневмонита – значительная перибронхиальная и периваскулярная воспалительная инфильтрация, утолщение межальвеолярных перегородок и гиперплазия эпителия бронхов), печени (дистрофические изменения гепатоцитов, воспалительная инфильтрация перипортальных трактов и начальные признаки фиброза), почках (признаки мембранозного гломерулонефрита – утолщение базальных мембран капилляров клубочков и выраженная дистрофия эпителия проксимальных канальцев), миокарде (дистрофические изменения кардиомиоцитов сердца) и селезёнке (гипоплазия или гиперплазия отдельных лимфофолликулов).
- Ингаляционное воздействие КГ в концентрации 4,4 мг/м³ вызывало менее распространённые и более слабые проявления токсического действия, характеризующиеся умеренным повышением билирубина и снижением уровня холестерина в сыворотке крови, минимальными структурными изменениями в бронхах (очаговая гиперплазия бокаловидных клеток) и лёгочной паренхиме (слабовыраженная периваскулярная и перибронхиальная воспалительная инфильтрация, незначительное утолщение межальвеолярных перегородок) в сочетании с реактивными изменениями селезёнки животных.
- У опытных животных после хронического воздействия КГ в концентрации 1,6 мг/м³ все изученные морфофункциональные показатели и гистологические характеристики внутренних органов не имели существенных различий с таковыми у контрольных животных.
- На основании результатов ингаляционного эксперимента концентрация КГ 4,4 мг/м³ принята пороговой хронического токсического действия – более чем в три раза ниже ранее установленных величин пороговых концентраций субхронического специфического дисбиотического и аллергического действий. Это определило как критерий гигиенического нормирования КГ ведущее вредное общетоксическое действие на организм. С учётом рассчитанного коэффициента запаса (11) к пороговой концентрации хронического токсического действия обоснована ПДКврз аэрозоля клиндамицина гидрохлорида на уровне 0,4 мг/м³, что соответствует II классу опасности.
Ограничения исследования. Исследования ограничены изучением токсического действия фармацевтической субстанции КГ в хроническом эксперименте при ингаляционном воздействии. Результаты исследования применимы для обоснования предельно допустимой концентрации исследуемой субстанции в воздухе рабочей зоны (ПДКврз).
Заключение
В результате хронического ингаляционного эксперимента установлено, что концентрация КГ на уровне 13,5 мг/м³ является эффективно действующей по токсическому эффекту, концентрация КГ на уровне 4,4 мг/м³ признана пороговой по токсическому действию на организм, а концентрация 1,6 мг/м³ является недействующей.
При обосновании ПДКврз фармацевтической субстанции КГ исходили из лимитирующих порогов вредного действия на организм, установленных при изучении специфического дисбиотического и аллергического, токсического действия препарата в ингаляционных экспериментах [10, 12, 15]. При этом установленная величина пороговой концентрации хронического токсического действия КГ (4,4 мг/м³) более чем в три раза ниже ранее определённых в субхроническом ингаляционном эксперименте величин пороговых концентраций КГ по специфическому дисбиотическому (13,5 ± 0,4 мг/м³) и аллергическому (27,5 ± 0,8 мг/м³) действиям [10, 11]. Следовательно, критерием гигиенического нормирования КГ является ведущее вредное общетоксическое действие на организм. На этом основании с учётом рассчитанного коэффициента запаса [16] к пороговой концентрации хронического токсического действия обоснована ПДКврз аэрозоля клиндамицина гидрохлорида на уровне 0,4 мг/м³, что соответствует II классу опасности [16–18].
Список литературы
1. Василькевич В.М., Богданов Р.В., Дроздова Е.В. Актуальные вопросы гигиенического регламентирования и создания безопасных условий труда на предприятиях по производству фармацевтических препаратов. Медицина труда и промышленная экология. 2020; 60(10): 640–4. https://doi.org/10.31089/1026-9428-2020-60-10-640-644 https://elibrary.ru/ynajfr
2. Бухтияров И.В. Современное состояние и основные направления сохранения и укрепления здоровья работающего населения России. Медицина труда и промышленная экология. 2019; 59(9): 527–32. https://doi.org/10.31089/1026-9428-2019-59-9-527-532 https://elibrary.ru/htkrsy
3. Сычик С.И., Шевляков В.В. Развитие концепции и методологии гигиенического нормирования белоксодержащих аэрозолей в воздухе рабочей зоны. Здоровье и окружающая среда. 2018; (28): 163–7. https://elibrary.ru/zqchjd
4. Сычик С.И. Некоторые итоги и концептуальные направления научных исследований и нормативно-методического обеспечения государственного санитарного надзора по проблеме медицины труда в Республике Беларусь. В кн.: Материалы XII Всероссийского конгресса «Профессия и здоровье» и V Всероссийского съезда врачей-профпатологов. М.; 2013: 439–41.
5. Земцова В.О., Богданов Р.В., Шевляков В.В. Экспериментальная оценка острой токсичности фармацевтической субстанции клиндамицина гидрохлорида. В кн.: Здоровье и окружающая среда: сборник материалов международной научно-практической конференции, посвященной 95-летию республиканского унитарного предприятия «Научно-практический центр гигиены». Минск; 2022: 447–50. https://elibrary.ru/oeqymb
6. Регистр лекарственных средств России. Клиндамицин (Clindamycinum). Доступно: https://rlsnet.ru/drugs/klindamicin-1663
7. Постановка исследований для обоснования предельно допустимых концентраций антибиотиков в воздухе рабочей зоны: методические указания № 5051-89, утвержденные заместителем государственного санитарного врача СССР. М.; 1989.
8. Методические указания МУ 11-11-10 РБ-02. Требования к постановке токсиколого-аллергологических исследований при гигиеническом нормировании белоксодержащих аэрозолей в воздухе рабочей зоны. Минск; 2002.
9. Земцова В.О., Шевляков В.В., Богданов Р.В., Василькевич В.М. Особенности биологического действия фармацевтической субстанции клиндамицина гидрохлорид в субхроническом эксперименте. В кн.: Сборник статей и тезисов. Медицинская наука: вчера, сегодня, завтра. М.; 2024: 1774–1780.
10. Земцова В.О., Богданов Р.В., Шевляков В.В., Филонюк В.А., Емельянова О.А., Эрм Г.И. и др. Экспериментальная оценка токсического, аллергического и дисбиотического действия на организм фармацевтической субстанции клиндамицин гидрохлорид при субхроническом ингаляционном воздействии. Здоровье и окружающая среда. 2024; (34): 200–9. https://elibrary.ru/dslrsg
11. Земцова В.О., Богданов Р.В., Шевляков В.В., Филонюк В.А., Чернышова Е.В., Баранов С.А. Оценка степени сенсибилизирующей способности и аллергенной опасности фармацевтической субстанции клиндамицина гидрохлорид в экспериментах на белых мышах. БГМУ в авангарде медицинской науки и практики. 2024; 14(2): 110–6.
12. Земцова В.О., Богданов Р.В., Шевляков В.В., Филонюк В.А., Емельянова О.А., Чернышова Е.В. и др. Обоснование и апробация методических подходов экспериментальной оценки острого дисбиотического действия антибактериальных лекарственных средств. Здоровье и окружающая среда. 2024; (34): 209–16. https://elibrary.ru/jgshkr
13. Земцова В.О., Богданов Р.В., Шевляков В.В., Эрм Г.И. Экспериментальная оценка острой токсичности фармацевтических субстанций антибактериальных лекарственных средств. В кн.: Здоровье и окружающая среда: сборник материалов международной научно-практической конференции. Минск; 2023: 405–9. https://elibrary.ru/rgvohd
14. Буеверов А.О., Богомолов П.О., Буеверова Е.Л. Гепатотоксичность антибактериальных препаратов в терапевтической практике. Клиническая микробиология и антимикробная химиотерапия. 2015; 17(3): 207–16. https://elibrary.ru/uhpuxj
15. Обоснование предельно допустимых концентраций и методик выполнения измерений содержания в воздухе рабочей зоны микроорганизмов-продуцентов и микробных препаратов на их основе: инструкция по применению № 009-1015. Минск; 2015.
16. Метод гигиенического нормирования содержания антибактериальных лекарственных средств в воздухе рабочей зоны: инструкция по применению № 034-1124. Минск; 2024.
17. Филонюк В.А., Шевляков В.В., Дудчик Н.В. Методология гигиенического регламентирования микробных препаратов и разработки методик выполнения измерений содержания микроорганизмов в воздухе рабочей зоны. Минск: Транстехника; 2018.
18. Гигиенический норматив «Показатели безопасности и безвредности микроорганизмов-продуцентов, микробных препаратов и их компонентов, вредных веществ в воздухе рабочей зоны и на кожных покровах работающих». Минск; 2021.
Об авторах
Виолетта Олеговна ЗемцоваБеларусь
Аспирант, научный сотрудник лаборатории промышленной токсикологии Научно-исследовательского института гигиены, токсикологии, эпидемиологии, вирусологии и микробиологии государственного учреждения «Республиканский центр гигиены, эпидемиологии и общественного здоровья», 220012, г. Минск, Республика Беларусь
e-mail: veto4ka1710@rambler.ru
Руслан Валерьевич Богданов
Беларусь
Кандидат мед. наук, заведующий лабораторией промышленной токсикологии Научно-исследовательского института гигиены, токсикологии, эпидемиологии, вирусологии и микробиологии государственного учреждения «Республиканский центр гигиены, эпидемиологии и общественного здоровья», 220012, г. Минск, Республика Беларусь
e-mail: 7_rus@tut.by
Светлана Николаевна Рябцева
Беларусь
Кандидат мед. наук, доцент, заведующий лабораторией центр морфологических исследований Института физиологии Национальной академии наук Беларуси, 220072, г. Минск, Республика Беларусь
e-mail: sveta.rjabceva@tut.by
Виталий Васильевич Шевляков
Беларусь
Доктор мед. наук, профессор, главный научный сотрудник лаборатории промышленной токсикологии Научно-исследовательского института гигиены, токсикологии, эпидемиологии, вирусологии и микробиологии государственного учреждения «Республиканский центр гигиены, эпидемиологии и общественного здоровья», 220012, г. Минск, Республика Беларусь
e-mail: shev-vitaliy@mail.ru
Сергей Иванович Сычик
Беларусь
Кандидат мед. наук, доцент, директор Научно-исследовательского института гигиены, токсикологии, эпидемиологии, вирусологии и микробиологии государственного учреждения «Республиканский центр гигиены, эпидемиологии и общественного здоровья», 220012, г. Минск, Республика Беларусь
e-mail: rspch@rspch.by
Елена Вадимовна Чернышова
Беларусь
Кандидат мед. наук, ведущий научный сотрудник лаборатории промышленной токсикологии Научно-исследовательского института гигиены, токсикологии, эпидемиологии, вирусологии и микробиологии государственного учреждения «Республиканский центр гигиены, эпидемиологии и общественного здоровья», 220012, г. Минск, Республика Беларусь
e-mail: merald_25@mail.ru
Рецензия
Для цитирования:
Земцова В.О., Богданов Р.В., Рябцева С.Н., Шевляков В.В., Сычик С.И., Чернышова Е.В. Обоснование гигиенического норматива содержания в воздухе рабочей зоны фармацевтической субстанции клиндамицина гидрохлорида с учётом его токсических свойств, подтверждённых в хроническом ингаляционном эксперименте. Токсикологический вестник. 2025;33(6):493-501. https://doi.org/10.47470/0869-7922-2025-33-6-493-501. EDN: qujovi
For citation:
Zemtsova V.O., Bogdanov R.V., Rjabceva S.N., Shevlyakov V.V., Sychik S.I., Chernyshova E.V. Justification of the hygienic standard for the content of the pharmaceutical substance clindamycin hydrochloride in the air of the working area, taking into account its toxic properties, confirmed in a chronic inhalation experiment. Toxicological Review. 2025;33(6):493-501. (In Russ.) https://doi.org/10.47470/0869-7922-2025-33-6-493-501. EDN: qujovi
JATS XML





































