Перейти к:
Подходы к оценке in vitro генотоксичного потенциала наноматериалов (на примере углеродных нанотрубок)
https://doi.org/10.47470/0869-7922-2026-34-1-5-15
EDN: sxhqvv
Аннотация
Введение. Углеродные нанотрубки (УНТ) – высокотехнологичные материалы, однако их генотоксический и канцерогенный потенциал изучен недостаточно. Для оценки генотоксичности УНТ необходимы альтернативные методы in vitro, разработка которых невозможна без предварительного изучения механизмов повреждения ДНК.
Материал и методы. Исследование проведено на 2D- и 3D-культурах клеток дыхательной системы человека. Исследованы эффекты российских одностенных (ОУНТ TUBALL™, очищенные и неочищенные) и многостенных (МУНТ «Таунит-М») УНТ. Цитотоксичность УНТ оценивали с помощью MTS-теста и анализа лактатдегидрогеназы (ЛДГ). Генотоксический потенциал исследовали методом ДНК-комет. Локализацию УНТ в клетках определяли методом просвечивающей электронной микроскопии. Для выявления окислительного стресса измеряли уровень активных форм кислорода (АФК) с использованием набора DCFDA. Профиброгенную и проапоптотическую активность УНТ определяли по экспрессии генов (TGF-β1, P53, Bax, Bcl2) методом ПЦР в реальном времени.
Результаты. Наибольшую чувствительность к цитотоксичности УНТ показали фибробласты, наименьшую – клетки A549. Генотоксичность УНТ выявлена на всех клетках при концентрации 20 мкг/мл. Все УНТ проникали в клетки, МУНТ обнаруживались в ядре клеток. Окислительный стресс дозозависимо индуцировался всеми типами УНТ, неочищенные ОУНТ вызывали наиболее выраженный эффект. В клетках BEAS-2B МУНТ вызывали повышение экспрессии TGF-β1 при низких концентрациях, в то время как ОУНТ вызывали аналогичный эффект лишь при высокой концентрации. В клетках A549 все типы УНТ проявляли профиброгенный эффект во всех концентрациях. В фибробластах значимого повышения экспрессии гена TGF-β1 не наблюдалось. В клетках BEAS-2B и A549 УНТ демонстрировали способность к инициации апоптотических сигнальных путей, в MRC5-SV40 признаков апоптоза в ответ на воздействие УНТ не выявлено. Исследования на 3D-моделях клеточных культур продемонстрировали признаки окислительного стресса в ответ на воздействие УНТ, проапоптотических и профиброгенных эффектов УНТ обнаружено не было.
Заключение. Генотоксичность УНТ определяется их типом и видом клеток-мишеней, проявляясь в субтоксическом диапазоне концентраций. Ключевые механизмы включают окислительный стресс, прямое повреждение ДНК и индукцию апоптоза. Результаты, полученные на 3D-моделях, демонстрируют меньшую чувствительность, что может указывать на защитную роль тканевой организации.
Ограничения исследования. В рамках данной работы не оценивалась возможная роль репарации ДНК. Исследование охватывает ограниченное число конкретных типов отечественных УНТ.
Соблюдение этических стандартов. Исследование не требует предоставления заключения комитета по биомедицинской этике или иных документов.
Участие авторов:
Фатхутдинова Л.М. – дизайн исследования, анализ материала, редактирование;
Тимербулатова Г.А. – культивирование клеток, проведение тестов на клетках, обобщение полученных результатов, редактирование;
Габидинова Г.Ф. – разработка подходов культивирования трёхмерных моделей, проведение тестов на клетках, обзор литературы, статистическая обработка данных, обобщение полученных результатов.
Все соавторы – утверждение окончательного варианта статьи, ответственность за целостность всех её частей.
Конфликт интересов. Авторы заявляют об отсутствии явных и потенциальных конфликтов интересов в связи с публикацией данной статьи.
Финансирование. Исследование выполнено при поддержке Российского научного фонда № 22-25-00512. https://rscf.ru/project/22-25-00512/
Поступила в редакцию: 22 января 2026 / Принята в печать: 02 февраля 2026 / Опубликована: 18 марта 2026
Ключевые слова
Для цитирования:
Фатхутдинова Л.М., Тимербулатова Г.А., Габидинова Г.Ф. Подходы к оценке in vitro генотоксичного потенциала наноматериалов (на примере углеродных нанотрубок). Токсикологический вестник. 2026;34(1):5-15. https://doi.org/10.47470/0869-7922-2026-34-1-5-15. EDN: sxhqvv
For citation:
Fatkhutdinova L.M., Timerbulatova G.A., Gabidinova G.F. Approaches to the in vitro assessment of the genotoxic potential of carbon nanotubes. Toxicological Review. 2026;34(1):5-15. (In Russ.) https://doi.org/10.47470/0869-7922-2026-34-1-5-15. EDN: sxhqvv
Введение
Одностенные (ОУНТ) и многостенные (МУНТ) углеродные нанотрубки представляют собой класс высокотехнологичных материалов с уникальными механическими, электрическими и термическими свойствами, что обусловливает расширение их применения в составе композитных материалов, электронике, биомедицине и других областях [1, 2]. Вместе с этим растёт и потенциал воздействия наноматериалов на человека, преимущественно через дыхательную систему [3].
Вопрос о безопасности УНТ, их канцерогенном и генотоксическом потенциале остаётся дискуссионным [4]. Международное агентство по изучению рака (IARC) классифицировало определённые типы МУНТ (Mitsui-7) как возможный канцероген для человека (группа 2B) [5]. Генотоксичность как способность химических или физических агентов повреждать генетический материал клетки может явиться ключевым событием в инициации канцерогенеза и развитии наследственных болезней [6]. Однако генотоксический потенциал многих коммерчески производимых УНТ, в том числе отечественных, изучен недостаточно.
Наряду с изучением конечных точек генотоксичности для определения практического приложения результатов важно установление механизмов генотоксического действия. Потенциальные механизмы генотоксичности наноматериалов, в том числе УНТ, могут быть прямыми (физическое взаимодействие с ДНК или компонентами митотического аппарата) или косвенными, опосредованными через индукцию окислительного стресса, воспаления или нарушение процессов репарации ДНК [7–10].
Многочисленные экспериментальные данные, полученные как in vivo, так и in vitro, свидетельствуют о способности УНТ индуцировать фиброз [11, 12–17]. Накопленные данные указывают на тесную связь между фиброзом и канцерогенезом [11]. Предположительно, профиброгенная активность УНТ может представлять собой дополнительный механизм, способствующий развитию злокачественных новообразований.
В ряде исследований in vitro продемонстрировано, что различные типы УНТ способны индуцировать апоптоз; при этом было зафиксировано, что апоптотические процессы под воздействием УНТ часто сопровождались повреждением ДНК. Полученные данные позволяют сделать вывод о способности различных УНТ индуцировать апоптоз и параллельном проявлении ими генотоксической активности [18, 19].
Необходимость оценки в короткие сроки опасности для здоровья человека промышленно производимых наноматериалов и наносодержащей продукции, номенклатура которых ежегодно расширяется, затрудняет использование классических токсикологических методов исследования in vivo, требующих значительных временных, трудовых затрат и больших материальных ресурсов [19]. Современные подходы к оценке токсичности диктуют необходимость разработки и валидации альтернативных методов in vitro (например, с использованием клеточных культур), частично заменяющих эксперименты на животных [20]. Культуры клеток, в том числе усовершенствованные 3D-модели (сфероиды), могут использоваться для экспериментального выявления молекулярно-клеточных механизмов и особенностей действия наноматериалов при контакте с биологическими объектами [21, 22].
Цель настоящей работы – оценка генотоксического потенциала ОУНТ и МУНТ российского производства в экспериментах in vitro на 2D- и 3D-клетках эпителия и фибробластов дыхательной системы человека, а также исследование ключевых механизмов, лежащих в основе генотоксического действия УНТ, для последующей разработки подходов к оценке генотоксического потенциала УНТ в экспериментах in vitro.
Материал и методы
Исследования проведены на 2D-культурах клеток дыхательной системы человека: BEAS-2B (иммортализированные клетки бронхиального эпителия человека) (Cell Applications, Inc., США); A549 (клетки аденокарциномы альвеолярного эпителия лёгких человека) (CLS Cell Lines Service, Германия) и MRC5-SV40 (иммортализированные фибробласты лёгких человека, трансформированные SV40) (клетки предоставлены Черняком Б.В., НИИ физической химии им. А.Н. Белозерского МГУ). Клетки культивировали в среде DMEM с добавлением 10% эмбриональной бычьей сыворотки, 100 Ед/мл пенициллина и 100 мкг/мл стрептомицина в инкубаторе при температуре плюс 37 °C и 5%-м содержании CO2.
Для формирования 3D-сфероидов клетки высевали в 96-луночные планшеты с покрытием, препятствующем адгезии, и круглым дном (Cell Floater, SPL Lifesciences, Корея) [23]. Исследовали совместные культуры клеток бронхиального эпителия BEAS-2B и фибробластов лёгких человека MRC5-SV40.
В качестве материалов для исследования использованы одностенные углеродные нанотрубки TUBALL™ производства группы компаний OCSiAl (Новосибирск, Россия) в двух вариантах: очищенные и не очищенные от металлических примесей, а также многостенные углеродные нанотрубки «Таунит-М» производства ООО «НаноТехЦентр» (Тамбов, Россия).
Суспензии УНТ для экспериментов готовили в культуральной среде DMEM (Панеко, С410п, Россия) с добавлением 10% эмбриональной бычьей сыворотки (BioSera, Южная Америка) и подвергали ультразвуковой соникации при помощи прибора Sonic Vibra Cell Sonicator (Sonics&Materials, США). Были подобраны следующие параметры работы прибора: 750 Ватт, 20 кГц, 40% амплитуда, пульс 5/6, время 30 минут непосредственно перед внесением в культуру клеток [24].
Диапазоны концентраций УНТ для экспериментов in vitro были определены на основе данных, полученных при исследовании содержания УНТ в воздухе рабочей зоны предприятий, производящих исследуемые наноматериалы, а также сведений из научной литературы, описывающих как нетоксичные, так и потенциально токсичные концентрации УНТ.
Цитотоксичность УНТ определяли с помощью MTS-теста (Promega, США), оценивающего метаболическую активность и жизнеспособность клеток, и анализа лактатдегидрогеназы (ЛДГ) (набор для анализа ЛДГ, Abcam, Великобритания), определяющего целостность плазматической мембраны.
Для MTS-теста клетки инкубировали с 18 концентрациями (от 0.0006 до 200 мкг/мл) для каждого типа исследуемых УНТ в течение 72 часов. Оптическая плотность образцов в трёх повторах оценивалась с помощью микропланшетного фотометра Multiskan™ FC (Thermo Fisher Scientific, США) при длине волны 492 нм. При анализе результатов MTS-теста считалось, что УНТ обладают цитотоксическим потенциалом, проявляемым в отношении клеток, если жизнеспособность клеточной культуры снижалась до ≤ 70% по сравнению с контролем, для которого жизнеспособность условно принималась за 100%.
Для анализа активности ЛДГ исследуемые клетки подвергали воздействию четырёх концентраций каждого типа УНТ (100, 50, 0.03 и 0.0006 мкг/мл) в течение 72 ч. Активность ЛДГ, высвободившейся в культуральную среду, определяли с использованием набора LDH Assay Kit (Аbcam, UK (Великобритания)) согласно протоколу производителя. Оптическую плотность образцов в трёх повторах определяли на микропланшетном фотометре Multiskan™ FC (Thermo Fisher Scientific, США).
Генотоксичность оценивали с использованием щелочного варианта теста ДНК-комет (Trevigen, США). В эксперименте использованы две концентрации УНТ (20 и 0.0006 мкг/мл) при инкубации 72 ч. В качестве положительного контроля использовали доксорубицин в концентрации 1 мМ/мл, в качестве отрицательного контроля – клетки без воздействия УНТ. После окрашивания флуоресцентным красителем SybrGreen (Invitrogen, США) клетки визуализировали на флуоресцентном микроскопе Olympus BX63 (Япония) при длине волны 425–500 нм. Цифровые изображения анализировали в программе CaspLab (v.1.2.3), оценивая не менее 100 случайных комет на образец. Результаты выражали в процентах ДНК в хвосте кометы (% ДНК в хвосте кометы).
Локализацию УНТ в клетках анализировали методом просвечивающей электронной микроскопии после инкубации клеток с дисперсией исследуемых УНТ в концентрации 100 мкг/мл в течение 72 часов. Визуализацию образцов проводили с помощью просвечивающего электронного микроскопа Hitachi HT 7700 Exalens (Hitachi, Япония).
Уровень активных форм кислорода (АФК) в клетках измеряли с помощью набора для анализа активных форм кислорода DCFDA (Abcam, Великобритания) после 72 ч инкубации клеток с УНТ в пяти концентрациях (100, 50, 20, 0.03, 0.0006 мкг/мл). Флуоресценцию образцов в трёх повторах измеряли при длине волны 485 нм с помощью микропланшетного ридера Varioskan LUX (Thermo Fisher Scientific, Германия).
Профиброгенную и проапоптическую активность УНТ оценивали с помощью анализа экспрессии генов методом ПЦР в режиме реального времени. Уровни мРНК профибротического гена TGF-β1, маркёров апоптоза P53, Bax и Bcl2 оценивали в клетках, подвергнутых воздействию четырёх концентраций (100, 50, 0.03, 0.0006 мкг/мл) всех типов УНТ после 72 часов воздействия. Каждый образец анализировали в трёх повторностях. Расчёт оценки уровня мРНК генов проводили методом 2–ΔΔCt относительно контроля для каждой клеточной линии.
Статистическую обработку данных выполняли с использованием программы Microsoft Excel 2016 и пакета R [25]. Для оценки достоверности различий применяли t-критерий Стьюдента, различия при p < 0.05 считали статистически значимыми. Результаты представлены в формате M ± SD (среднее арифметическое ± стандартное отклонение). Интегральную оценку уровня мРНК генов – маркёров фиброза и апоптоза проводили с помощью анализа главных компонент.
Результаты
Определение диапазона концентраций для экспериментов in vitro. Данные о содержании УНТ в воздухе рабочей зоны предприятий, производящих исследуемые наноматериалы, были использованы для расчёта диапазона концентраций в экспериментах in vitro [19, 26]. С учётом данных, полученных при компьютерном моделировании депонирования аэрозоля УНТ в различных отделах лёгких человека (с использованием программного обеспечения MPPD (Multiple Path Particle Dosimetry V3.04) [27]) и данных открытых источников литературы, диапазон концентраций для исследования составил 0,0006–200 мкг/мл. Нижний предел диапазона (0,0006 мкг/мл) соответствует реальной производственной экспозиции ОУНТ, а 0,03 мкг/мл – производственной экспозиции МУНТ.
С целью выбора соответствующего диапазона концентраций для дальнейших экспериментов перед оценкой генотоксичности исследовали цитотоксичность наноматериалов.
Оценка цитотоксичности. Оценка жизнеспособности клеток выявила значительные различия в чувствительности к УНТ в зависимости от типа клеток и наноматериала.
Для клеток бронхиального эпителия BEAS-2B порог цитотоксичности (снижение жизнеспособности до ≤ 70%), по данным MTS-теста, составлял 100 мкг/мл для МУНТ и неочищенных ОУНТ, 50 мкг/мл – для очищенных ОУНТ. Анализ активности лактатдегидрогеназы подтвердил дозозависимое увеличение цитотоксического эффекта в тех же диапазонах концентраций.
Клетки A549 проявили наименьшую чувствительность: ни один из типов УНТ в исследованном диапазоне (до 200 мкг/мл) не привёл к значимому снижению жизнеспособности (по данным MTS-теста и анализа ЛДГ).
Фибробласты лёгких MRC5-SV40 были наиболее чувствительной линией. По данным MTS теста, цитотоксические эффекты МУНТ наблюдались уже при концентрации 0,1 мкг/мл, в то время как для очищенных и неочищенных ОУНТ порог составлял 6 мкг/мл. Данные ЛДГ-теста на клетках MRC5-SV40 свидетельствовали о цитотоксической активности УНТ во всех четырёх исследуемых концентрациях.
На основании этих данных для последующей оценки генотоксичности были выбраны две конечные точки, на которых потенциальная фрагментация ДНК при цитотоксичности не влияет на результаты теста ДНК-комет: нецитотоксическая концентрация (0,0006 мкг/мл), при которой жизнеспособность всех линий сохранялась на уровне ≥ 75%, и субтоксическая концентрация (20 мкг/мл), при которой жизнеспособность составляла ≥ 55% (на границе или ниже порога цитотоксичности для MRC5-SV40).
Оценка генотоксичности. В клетках бронхиального эпителия, альвеолярного эпителия и фибробластах лёгких воздействие всех видов УНТ в концентрации 0,0006 мкг/мл, соответствующей производственной экспозиции, и при 72-часовой инкубации не вызвала значимого повышения процентного содержания ДНК в хвосте комет.
В клеточной линии бронхиального эпителия BEAS-2B при воздействии УНТ в концентрации 20 мкг/мл наблюдалось значимое повышение содержания ДНК в хвосте кометы (p < 0.05), при этом МУНТ и не очищенные от металлических примесей ОУНТ вызывали более высокую степень повреждения ДНК по сравнению с очищенными ОУНТ.
Несмотря на отсутствие цитотоксических эффектов в клетках линии А549 вплоть до концентрации 200 мкг/мл, результаты теста ДНК-комет также продемонстрировали значимое повышение уровня повреждения генетического материала при воздействии всех видов УНТ в концентрации 20 мкг/мл (p < 0,05), при этом процентное содержание ДНК в хвосте кометы в клетках, инкубированных с УНТ, оказалось сопоставимо с положительным контролем – доксорубицинином в концентрации 1 мМ/мл.
Воздействие МУНТ и очищенных ОУНТ в концентрации 20 мкг/мл вызывало значимое повышение доли ДНК в хвосте кометы в клетках MRC5-SV40 по сравнению с отрицательным контролем (p < 0.05), при этом воздействие неочищенных ОУНТ не индуцировало такого эффекта.
Оценка проникновения УНТ в клетки. При изучении проникновения УНТ в клетки линии BEAS-2B были получены ПЭМ-изображения стадии эндоцитоза. МУНТ образуют большие скопления у плазматической мембраны клеток, единичные нанотрубки и спутанные клубки нанотрубок захватывались клетками. ОУНТ были более склонны к группированию в виде пучков, что может затруднять проникновение в клетки ввиду их длины. МУНТ также показали накопление в клетке в виде лизосомоподобных структур, где они выглядят более агрегированными, чем вне клетки.
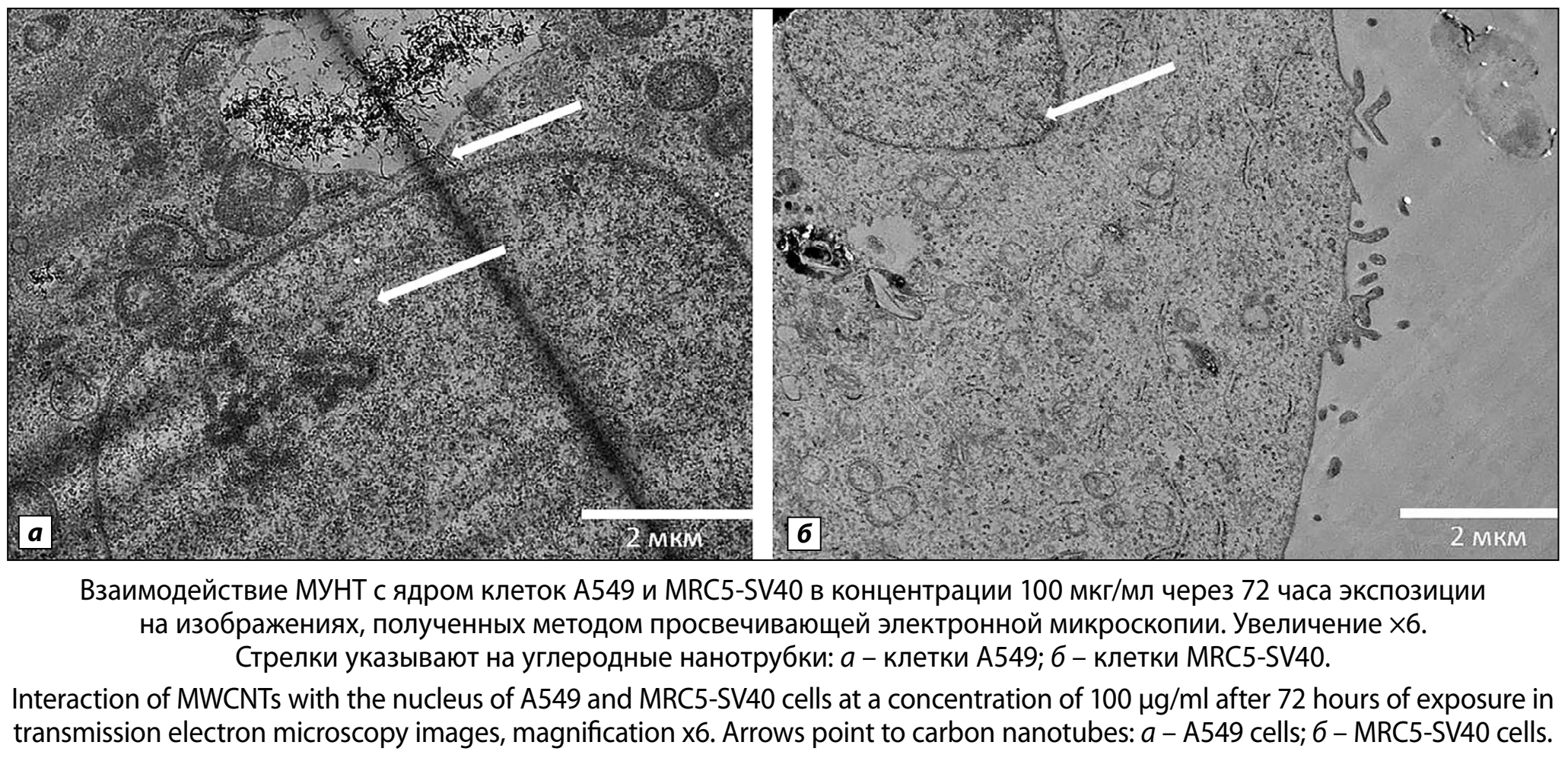
Такие же результаты были получены при изучении проникновения УНТ в клетки альвеолярного эпителия. Кроме этого, выявлено взаимодействие МУНТ с ядерной мембраной клеток альвеолярного эпителия: наночастицы образуют скопления вблизи ядерной мембраны клеток и проникают сквозь неё, единичные МУНТ обнаружены внутри ядра, что свидетельствует о возможном прямом воздействии данного вида УНТ на ДНК (рисунок, а).
Аналогичные результаты были получены в фибробластах MRC5-SV40: УНТ также проникают в клетки, при этом МУНТ имеют тенденцию образовывать кластеры в цитоплазме клеток. Обнаружены одиночные МУНТ, проникающие в ядерную мембрану клеток MRC5-SV40 (рисунок, б).
Оценка прооксидантных свойств УНТ. По результатам теста DCFH-DA установлено, что во всех клеточных культурах происходило дозозависимое увеличение уровня активных форм кислорода при действии всех типов УНТ, при этом значимое повышение по сравнению с отрицательным контролем наблюдалось начиная с концентрации 20 мкг/мл (табл. 1).
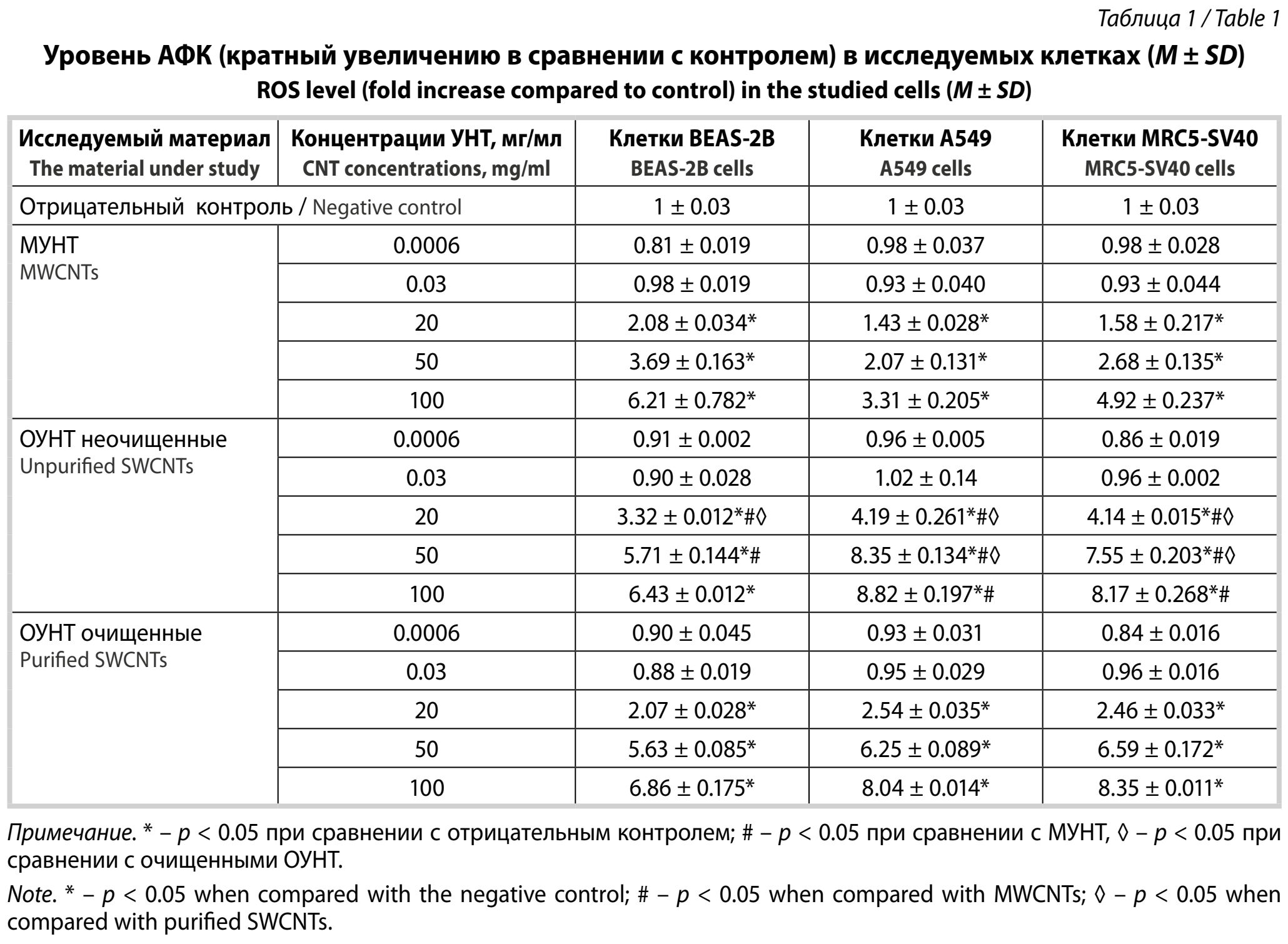
Воздействие неочищенных ОУНТ по сравнению с МУНТ приводило к более высокому уровню окислительного стресса: в клетках BEAS-2B при концентрациях 20 и 50 мкг/мл с выравниванием эффектов при концентрации 100 мкг/мл, в клетках A549 и MRC5-SV40 – в диапазоне концентраций 20–100 мкг/мл. Кроме того, неочищенные ОУНТ продемонстрировали более высокий окислительный потенциал по сравнению с очищенными ОУНТ при концентрациях 20 и 50 мкг/мл.
Оценка профиброгенных эффектов УНТ. При оценке экспрессии гена TGF-β1, участвующего в патогенезе фиброза, в клетках бронхиального эпителия установлено, что МУНТ в концентрациях 0,0006 и 0,03 мкг/мл при 72-часовом воздействии вызывали повышение экспрессии гена, свидетельствующее о потенциальном профиброгенном эффекте. Для двух типов ОУНТ повышение экспрессии гена TGF-β1 наблюдалось при концентрации 100 мкг/мл. В альвеолярных эпителиальных клетках A549 положительная экспрессия гена TGF-β1 наблюдалась при воздействии УНТ во всех концентрациях. Для фибробластов MRC5-SV40 обнаружено подавление экспрессии гена TGF-β1, что может рассматриваться как проявление регуляторной адаптации фибробластов. Обобщённые результаты представлены в табл. 2.

Оценка проапоптических эффектов УНТ. В клетках бронхиального эпителия BEAS-2B, подвергшихся воздействию УНТ, уровень экспрессии гена P53, играющего основную роль в регуляции транскрипции проапоптотических и антиапоптотических членов семейства белков BCL2, значимо не отличался от контроля (p > 0.05). При этом после экспозиции к МУНТ в концентрациях 0,0006 и 0,03 мкг/мл наблюдалось повышение экспрессии гена BAX (p <0,05), инициирующего апоптоз, и сниженная экспрессия антиапоптического гена BCL2 (p < 0,05); при более высоких концентрациях (50 и 100 мкг/мл) признаки апоптоза уже отсутствовали. Выраженность эффектов ОУНТ на клетках BEAS-2B отличалась от эффектов МУНТ: инициация апоптоза происходила лишь при воздействии высокой концентрации 100 мкг/мл неочищенных ОУНТ TUBALL™ – в первую очередь повышалась экспрессия проапоптотического гена BAX (p < 0,05). При экспозиции очищенных ОУНТ TUBALLTM снижалась экспрессия гена BCL2 (p < 0,05) с изменением баланса BAX/BCL2 до 2.68 при концентрации 100 мкг/мл, что указывает на возможность запуска процессов апоптоза.
В клетках альвеолярного эпителия A549 МУНТ статистически значимо повышали экспрессию гена Р53 по сравнению с контролем начиная с концентрации 0.03 мкг/мл (p < 0.05); статистически значимое увеличение экспрессии генов BAX и BCL2 (с повышением соотношения BAX/BCL2 до 1,5) наблюдалось при концентрации 100 мкг/мл (p < 0.05). Для неочищенных ОУНТ экспрессия гена Р53 статистически значимо повышалась уже при самой низкой концентрации – 0,0006 мкг/мл (p < 0.05), для очищенных ОУНТ – начиная с 0,03 мкг/мл (p < 0,05). При концентрации 100 мкг/мл признаки апоптоза отсутствовали, что может указывать на преобладание некротического пути гибели клеток. Во всём диапазоне концентраций соотношение BAX/BCL2 при экспонировании клеток A549 к ОУНТ было выше 1,0 (статистически значимо для неочищенных ОУНТ в концентрациях 0,0006 и 100 мкг/мл) (p < 0,05), что свидетельствует о преобладании проапоптотических процессов над антиапоптотическими.
В экспериментах с культурой фибробластов лёгких MRC5-SV40 признаков апоптоза при воздействии на клетки МУНТ обнаружено не было. Для ОУНТ, несмотря на положительную экспрессию гена Р53, наблюдалась тенденция к смещению соотношения BAX/BCL2 в сторону повышенной экспрессии антиапоптотического гена BCL2 во всём диапазоне изученных концентраций, что может свидетельствовать об ингибировании апоптоза.
Оценка цитотоксичности, прооксидантных, профиброгенных свойств и проапоптических эффектов УНТ на 3D-моделях клеток дыхательной системы человека. Культивирование 3D-моделей клеточных культур проводилось в соответствии с протоколом, описанным в ранее проведёном исследовании [23].
В трёхмерной ко-культуре BEAS-2B и MRC5-SV40 повышение активности ЛДГ под действием углеродных нанотрубок отмечалось только при высокой концентрации (100 мкг/мл) для МУНТ и неочищенных ОУНТ. Можно предположить, что взаимодействие эпителиальных клеток и фибробластов и их обмен сигналами ведут к формированию наиболее приближенного к нативной ткани микроокружения и включению защитных механизмов при воздействии УНТ. Эта закономерность не наблюдалась в случае очищенных ОУНТ, что может быть связано с размерами агломератов или другими механизмами реализации цитотоксичности, и это требует дальнейшего исследования.
В ко-культуре 3D-модели из клеток BEAS-2B и MRC5-SV40 воздействие МУНТ и очищенных ОУНТ вызывало статистически значимое повышение уровня активных форм кислорода по сравнению с контролем начиная с концентрации 20 мкг/мл. Для неочищенных ОУНТ было установлено, что при воздействии низких концентраций в клетках происходит значимое снижение уровня активных форм кислорода по сравнению с контролем с нарастанием с 20 мкг/мл и значимым увеличением только на 50 мкг/мл. В ко-культуре 3D-клеточных систем относительный уровень экспрессии гена TGF-β1 не повышался по сравнению с контролем при воздействии всех типов УНТ. В ко-культуре клеток 3D бронхиального эпителия BEAS-2B и лёгочных фибробластов MRC5-SV40 признаков апоптоза при экспозиции к каждому из изучавшихся типов УНТ также обнаружено не было.
Обсуждение
В настоящем исследовании было показано отсутствие генотоксического эффекта УНТ при концентрации, соответствующей производственной экспозиции (0,0006 мкг/мл). Однако для субтоксической концентрации УНТ 20 мкг/мл было выявлено увеличение числа нестабильных участков ДНК, что свидетельствует о дозозависимой генотоксичности этих материалов. Ранее исследования генотоксичности различных типов УНТ при более высоких концентрациях (от 80 мкг/мл и выше) показали противоречивые результаты, что может быть связано с различиями в чувствительности клеток к УНТ [28, 29], а также с физико-химическими характеристиками исследуемых УНТ [30].
В качестве механизмов генотоксичности УНТ в клетках дыхательной системы человека были исследованы генерация активных форм кислорода (АФК), прямое повреждение генетического материала при поглощении наноматериалов клеткой и хроническая персистенция УНТ внутри клетки и ядра. Кроме этого, были изучены профиброгенные эффекты и проапоптотический потенциал УНТ.
Генерация АФК широко признана основным механизмом, лежащим в основе генотоксичности [7]. Результаты анализа DCFH-DA продемонстрировали значительное увеличение внутриклеточной продукции АФК после 72 часов воздействия всех типов УНТ начиная с концентрации 20 мкг/мл. Подобные наблюдения повышенного окислительного стресса и генотоксических эффектов, вызванных воздействием УНТ, были зарегистрированы и другими исследовательскими группами для различных типов клеток, в том числе эпителиальных клеток бронхов человека BEAS-2B [30].
Были продемонстрированы особенности проникновения разных видов УНТ и накопления их в клетках дыхательной системы человека. Проникновение УНТ в клетки происходит преимущественно посредством эндоцитоза, при этом наночастицы могут локализоваться в лизосомоподобных структурах или свободно распределяться в цитоплазме клетки. Важным наблюдением является обнаруженная склонность МУНТ к накоплению вблизи ядерной мембраны и дальнейшее проникновение внутрь ядра, что стоит рассматривать как прямой механизм генотоксичности. Выявлены различия в проникновении ОУНТ и МУНТ в клетки: для последних были показаны склонность к образованию внутриклеточных скоплений и проникновение через ядерную мембрану. Данные, подтверждающие прямой контакт МУНТ и ОУНТ с ядром, немногочисленны и встречаются лишь в единичных публикациях [30, 31].
Изученные УНТ проявляют профиброгенные свойства в эпителиальных клетках BEAS-2B и A549. Было установлено увеличение экспрессии гена TGF-β1 в клетках бронхиального эпителия при нецитотоксических концентрациях МУНТ и высоких цитотоксических концентрациях неочищенных ОУНТ. Также было показано, что все типы УНТ при исследуемых концентрациях вызывали увеличение экспрессии профибротического фактора в клетках A549. Ни один из трёх типов УНТ не вызывал увеличения экспрессии TGF-β1 в фибробластах MRC5-SV40. Ранее в экспериментах in vitro с применением культуры фибробластов человека WI38-VA13 было установлено, что воздействие УНТ индуцирует дифференциацию фибробластов с трансформацией в миофибробласты [32]. Это может менять паттерн экспрессии генов и свидетельствовать о развитии регуляторной адаптации клеток, играющих ключевую роль в развитии фиброза. Данные результаты согласуются с предыдущими исследованиями, в которых воздействие МУНТ приводило к увеличению экспрессии гена TGF-β1 в клетках BEAS-2B [12, 17, 33]. Также была показана важная роль окислительного стресса в инициации фиброза [34–36]. В нес- кольких исследованиях продемонстрировано, что окислительный стресс, индуцированный УНТ, усиливает выработку и активацию профибротических факторов, в том числе TGF-β1 [12, 13, 36]. В совокупности эти данные позволяют предположить ключевую роль окислительного стресса как основного регулятора фиброгенеза, индуцированного УНТ.
Инициация апоптоза наблюдалась преимущественно при низких концентрациях УНТ. Так, МУНТ индуцировали апоптоз в клетках BEAS-2B, а неочищенные ОУНТ – в клетках A549 уже при минимальной концентрации, соответствующей производственной (0,0006 мкг/мл). Напротив, при высоких цитотоксических концентрациях в исследуемых клетках апоптоз не выявлялся. Отсутствие апоптоза при высоких цитотоксических концентрациях может объясняться доминированием альтернативных путей гибели клеток (некроз, некроптоз, аутофагия), которые опережают развитие апоптоза [37, 38]. При этом повреждение ДНК как известный фактор также может участвовать в инициации апоптоза [37].
Трёхмерные (3D) ко-культуры бронхиального эпителия и фибробластов продемонстрировали меньшую чувствительность к УНТ по сравнению с традиционными монослойными (2D) культурами. Результаты исследования токсичности УНТ на разработанных 3D-моделях продемонстрировали отсутствие проапоптотических и профиброгенных эффектов при концентрациях, соответствующих производственным экспозициям. Однако начиная с концентрации УНТ 20 мкг/мл, значительно превышающей концентрации, соответствующие производственным экспозициям, в клеточных моделях были обнаружены признаки окислительного стресса. При этом 3D-модели, приближенные по своим свойствам к нативной ткани, представляют собой эффективный скрининговый инструмент, снижающий риск ложноположительной оценки токсичности при переходе от экспериментов in vitro к in vivo.
Ограничения исследования. В рамках данной работы не оценивалась возможная роль репарации ДНК. Исследование охватывает ограниченное число конкретных типов отечественных УНТ.
Заключение
Исследование показало, что генотоксичность УНТ зависит от их типа и вида клеток, проявляясь преимущественно при субтоксических концентрациях. Ключевыми механизмами токсичности УНТ являются окислительный стресс, прямое взаимодействие с ДНК (для МУНТ) и индукция апоптоза. 3D-модели демонстрируют меньшую чувствительность, что может указывать на защитную роль тканевой организации.
Проведённая оценка генотоксического потенциала трех типов промышленных УНТ на 2D- и 3D-моделях клеток дыхательной системы человека позволила сформулировать принципы проведения подобных исследований. Необходимо использовать линейку тестов для выявления различных механизмов повреждения ДНК (прямое взаимодействие, оксидативный стресс, апоптоз, профиброгенный эффект). Обязательным является учёт клеточной специфичности, для чего в скрининг следует включать не менее двух различных типов клеток дыхательной системы как наиболее вероятного органа-мишени. Для повышения прогностической ценности данных и снижения риска гипердиагностики рекомендуется использовать продвинутые 3D-модели, в частности ко-культуры, в качестве следующего шага валидации результатов, полученных на традиционных 2D-моделях клеточных культур.
Список литературы
1. Mohd Nurazzi N., Asyraf M.R.M., Khalina A., Abdullah N., Sabaruddin F.A., Kamarudin S.H., et al. Fabrication, functionalization, and application of carbon nanotube-reinforced polymer composite: an overview. Polymers (Basel). 2021; 13(7): 1047. https://doi.org/10.3390/polym13071047
2. He H., Pham-Huy L.A., Dramou P., Xiao D., Zuo P., Pham-Huy C. Carbon nanotubes: applications in pharmacy and medicine. Biomed Res. Int. 2013; 2013: 578290. https://doi.org/10.1155/2013/578290
3. Guseva Canu I., Bateson T.F., Bouvard V., Debia M., Dion C., Savolainen K., et al. Human exposure to carbon-based fibrous nanomaterials: A review. Int. J. Hyg. Environ. Health. 2016; 219(2): 166–75. https://doi.org/10.1016/j.ijheh.2015.12.005
4. Donaldson K., Stone V., Seaton A., Tran L., Aitken R., Poland C. Re: Induction of mesothelioma in p53+/- mouse by intraperitoneal application of multi-wall carbon nanotube. J. Toxicol. Sci. 2008; 33(3): 385; author reply 386–8. https://doi.org/10.2131/jts.33.385
5. International Agency for Research on Cancer (IARC). Available at: https://iarc.who.int/
6. Takagi A., Hirose A., Futakuchi M., Tsuda H., Kanno J. Dose-dependent mesothelioma induction by intraperitoneal administration of multi-wall carbon nanotubes in p53 heterozygous mice. Cancer Sci. 2012; 103(8): 1440–4. https://doi.org/10.1111/j.1349-7006.2012.02318.x
7. Samadian H., Salami M.S., Jaymand M., Azarnezhad A., Najafi M., Barabadi H., et al. Genotoxicity assessment of carbon-based nanomaterials; Have their unique physicochemical properties made them double-edged swords? Mutat. Res. Rev. Mutat. Res. 2020; 783: 108296. https://doi.org/10.1016/j.mrrev.2020.108296
8. Sargent L.M., Hubbs A.F., Young S.H., Kashon M.L., Dinu C.Z., Salisbury J.L., et al. Single-walled carbon nanotube-induced mitotic disruption. Mutat. Res. 2012; 745(1-2): 28–37. https://doi.org/10.1016/j.mrgentox.2011.11.017
9. Shvedova A.A., Pietroiusti A., Fadeel B., Kagan V.E. Mechanisms of carbon nanotube-induced toxicity: Focus on oxidative stress. Toxicol. Appl. Pharmacol. 2012; 261(2): 121–33. https://doi.org/10.1016/j.taap.2012.03.023
10. Møller P., Christophersen D.V., Jensen D.M., Kermanizadeh A., Roursgaard M., Jacobsen N.R., et al. Role of oxidative stress in carbon nanotube-generated health effects. Arch. Toxicol. 2014; 88(11): 1939–64. https://doi.org/10.1007/s00204-014-1356-x
11. Dong J., Ma Q. Integration of inflammation, fibrosis, and cancer induced by carbon nanotubes. Nanotoxicology. 2019; 13(9): 1244–74. https://doi.org/10.1080/17435390.2019.1651920
12. He X., Young S.H., Schwegler-Berry D., Chisholm W.P., Fernback J.E., Ma Q. Multiwalled carbon nanotubes induce a fibrogenic response by stimulating reactive oxygen species production, activating NF-κB signaling, and promoting fibroblast-to-myofibroblast transformation. Chem. Res. Toxicol. 2011; 24(12): 2237–48. https://doi.org/10.1021/tx200351d
13. Manke A., Luanpitpong S., Dong C., Wang L., He X., Battelli L., et al. Effect of fiber length on carbon nanotube-induced fibrogenesis. Int. J. Mol. Sci. 2014; 15(5): 7444–61. https://doi.org/10.3390/ijms15057444
14. Mercer R.R., Scabilloni J.F., Hubbs A.F., Battelli L.A., McKinney W., Friend S., et al. Distribution and fibrotic response following inhalation exposure to multi-walled carbon nanotubes. Part. Fibre Toxicol. 2013; 10: 33. https://doi.org/10.1186/1743-8977-10-33
15. Shvedova A.A., Kisin E.R., Mercer R., Murray A.R., Johnson V.J., Potapovich A.I., et al. Unusual inflammatory and fibrogenic pulmonary responses to single-walled carbon nanotubes in mice. Am. J. Physiol. Lung Cell. Mol. Physiol. 2005; 289(5): 698–708. https://doi.org/10.1152/ajplung.00084.2005
16. Snyder-Talkington B.N., Dong C., Sargent L.M., Porter D.W., Staska L.M., Hubbs A.F., et al. mRNAs and miRNAs in whole blood associated with lung hyperplasia, fibrosis, and bronchiolo-alveolar adenoma and adenocarcinoma after multi-walled carbon nanotube inhalation exposure in mice. J. Appl. Toxicol. 2016; 36(1): 161–74. https://doi.org/10.1002/jat.3157
17. Wang X., Duch M.C., Mansukhani N., Ji Z., Liao Y.P., Wang M., et al. Use of a pro-fibrogenic mechanism-based predictive toxicological approach for tiered testing and decision analysis of carbonaceous nanomaterials. ACS Nano. 2015; 9(3): 3032–43. https://doi.org/10.1021/nn507243w
18. Nam C.W., Kang S.J., Kang Y.K., Kwak M.K. Cell growth inhibition and apoptosis by SDS-solubilized single-walled carbon nanotubes in normal rat kidney epithelial cells. Arch. Pharm. Res. 2011; 34(4): 661–9. https://doi.org/10.1007/s12272-011-0417-4
19. Patlolla A., Knighten B., Tchounwou P. Multi-walled carbon nanotubes induce cytotoxicity, genotoxicity and apoptosis in normal human dermal fibroblast cells. Ethn. Dis. 2010; 20(1 Suppl. 1): S1–65–72.
20. Гуськова О.А., Завьялов Н.В., Скворцова Е.Л., Хамидулина Х.Х. Сравнительная оценка исследования токсических свойств наноматериалов в экспериментах in vivo и in vitro. Токсикологический вестник. 2015; (1): 22–8. https://elibrary.ru/ywwcwq
21. NANoREG. Grant Agreement Number 310584. Deliverable D 2.06. Validated protocols for test item preparation for key in vitro and ecotoxicity studies; 2016.
22. Pfuhler S., van Benthem J., Curren R., Doak S.H., Dusinska M., Hayashi M., et al. Use of in vitro 3D tissue models in genotoxicity testing: Strategic fit, validation status and way forward. Report of the working group from the 7th International Workshop on Genotoxicity Testing (IWGT). Mutat. Res. Genet. Toxicol. Environ. Mutagen. 2020; 850–851: 503135. https://doi.org/10.1016/j.mrgentox.2020.503135
23. Габидинова Г.Ф., Тимербулатова Г.А., Убейкина Е.В., Саягфарова А.А., Фатхутдинова Л.М. Новые трёхмерные модели in vitro для оценки токсичности углеродных нанотрубок. Токсикологический вестник. 2023; 31(6): 352–62. https://doi.org/10.47470/0869-7922-2023-31-6-352-362 https://elibrary.ru/izuidk
24. Тимербулатова Г.А., Димиев А.М., Хамидуллин Т.Л., Бойчук С.В., Дунаев П.Д., Фахруллин Р.Ф. и др. Диспергирование одностенных углеродных нанотрубок в биосовместимых средах. Российские нанотехнологии. 2020; 15(4): 461–9. https://doi.org/10.1134/S1992722320040160 https://elibrary.ru/ntuimq
25. Гмошинский И.В., Хотимченко С.А., Ригер Н.А., Никитюк Д.Б. Углеродные нанотрубки: механизмы действия, биологические маркеры и оценка токсичности in vivo (обзор литературы). Гигиена и санитария. 2017; 96(2): 176–86. https://doi.org/10.18821/0016-9900-2017-96-2-176-186 https://elibrary.ru/yirfel
26. Fatkhutdinova L.M., Khaliullin T.O., Vasil‘yeva O.L., Zalyalov R.R., Mustafin I.G., Kisin E.R., et al. Fibrosis biomarkers in workers exposed to MWCNT. Toxicol. Appl. Pharmacol. 2016; 299: 125–31. https://doi.org/10.1016/j.taap.2016.02.016
27. Applied Research Associates. Multiple-Path Particle Dosimetry Model (MPPD v 3.04). Available at: https://ara.com/mppd/
28. Di Ianni E., Erdem J.S., Møller P., Sahlgren N.M., Poulsen S.S., Knudsen K.B., et al. In vitro-in vivo correlations of pulmonary inflammogenicity and genotoxicity of MWCNT. Part. Fibre Toxicol. 2021; 18(1): 25. https://doi.org/10.1186/s12989-021-00413-2
29. Lindberg H.K., Falck G.C., Singh R., Suhonen S., Järventaus H., Vanhala E., et al. Genotoxicity of short single-wall and multi-wall carbon nanotubes in human bronchial epithelial and mesothelial cells in vitro. Toxicology. 2013; 313(1): 24–37. https://doi.org/10.1016/j.tox.2012.12.008
30. Di Giorgio M.L., Di Bucchianico S., Ragnelli A.M., Aimola P., Santucci S., Poma A. Effects of single and multiwalled carbon nanotubes on macrophages: cyto and genotoxicity and electron microscopy. Mutat. Res. 2011; 722(1): 20–31. https://doi.org/10.1016/j.mrgentox.2011.02.008
31. Sargent L.M., Hubbs A.F., Young S.H., Kashon M.L., Dinu C.Z., Salisbury J.L., et al. Single-walled carbon nanotube-induced mitotic disruption. Mutat. Res. 2012; 745(1-2): 28–37. https://doi.org/10.1016/j.mrgentox.2011.11.017
32. Hindman B., Ma Q. Carbon nanotubes and crystalline silica induce matrix remodeling and contraction by stimulating myofibroblast transformation in a three-dimensional culture of human pulmonary fibroblasts: role of dimension and rigidity. Arch. Toxicol. 2018; 92(11): 3291–305. https://doi.org/10.1007/s00204-018-2306-9
33. Mishra A., Rojanasakul Y., Chen B.T., Castranova V., Mercer R.R., Wang L. Assessment of pulmonary fibrogenic potential of multiwalled carbon nanotubes in human lung cells. J. Nanomater. 2012; 13(1): 27. https://doi.org/10.1155/2012/930931
34. Azad N., Iyer A.K., Wang L., Liu Y., Lu Y., Rojanasakul Y. Reactive oxygen species-mediated p38 MAPK regulates carbon nanotube-induced fibrogenic and angiogenic responses. Nanotoxicology. 2013; 7(2): 157–68. https://doi.org/10.3109/17435390.2011.647929
35. Bargagli E., Olivieri C., Bennett D., Prasse A., Muller-Quernheim J., Rottoli P. Oxidative stress in the pathogenesis of diffuse lung diseases: a review. Respir. Med. 2009; 103(9): 1245–56. https://doi.org/10.1016/j.rmed.2009.04.014
36. Ma Q. Transcriptional responses to oxidative stress: pathological and toxicological implications. Pharmacol. Ther. 2010; 125(3): 376–93. https://doi.org/10.1016/j.pharmthera.2009.11.004
37. Mohammadinejad R., Moosavi M.A., Tavakol S., Vardar D.Ö., Hosseini A., Rahmati M., et al. Necrotic, apoptotic and autophagic cell fates triggered by nanoparticles. Autophagy. 2019; 15(1): 4–33. https://doi.org/10.1080/15548627.2018.1509171
38. Gmoshinsky I.V., Khotimchenko S.A., Riger N.A., Nikityuk D.B. Carbon nanotubes: mechanisms of the action, biological markers and evaluation of the (review of literature. Gigiena i Sanitaria (Hygiene and Sanitation, Russian journal). 2017; 96(2): 176–86. https://doi.org/10.18821/0016-9900-2017-96-2-176-186 https://elibrary.ru/yirfel (in Russian)
Об авторах
Лилия Минвагизовна ФатхутдиноваРоссия
Доктор медицинских наук, заведующий кафедрой гигиены, медицины труда ФГБОУ ВО Казанский государственный медицинский университет Минздрава России, 420012, г. Казань, Россия
e-mail: liliya.fatkhutdinova@kazangmu.ru
Гюзель Абдулхалимовна Тимербулатова
Россия
Доцент кафедры гигиены, медицины труда ФГБОУ ВО Казанский ГМУ Минздрава России, 420012, г. Казань, Россия
e-mail: guzel.timerbulatova@kazangmu.ru
Гульназ Фаезовна Габидинова
Россия
Ассистент кафедры гигиены, медицины труда ФГБОУ ВО Казанский ГМУ Минздрава России, 420012, г. Казань, Россия
e-mail: gabidinova26@kazangmu.ru
Рецензия
Для цитирования:
Фатхутдинова Л.М., Тимербулатова Г.А., Габидинова Г.Ф. Подходы к оценке in vitro генотоксичного потенциала наноматериалов (на примере углеродных нанотрубок). Токсикологический вестник. 2026;34(1):5-15. https://doi.org/10.47470/0869-7922-2026-34-1-5-15. EDN: sxhqvv
For citation:
Fatkhutdinova L.M., Timerbulatova G.A., Gabidinova G.F. Approaches to the in vitro assessment of the genotoxic potential of carbon nanotubes. Toxicological Review. 2026;34(1):5-15. (In Russ.) https://doi.org/10.47470/0869-7922-2026-34-1-5-15. EDN: sxhqvv
JATS XML





































