Перейти к:
Проблемы выявления эпигенетически активных негенотоксичных канцерогенов
https://doi.org/10.47470/0869-7922-2026-34-1-27-36
EDN: ikmcpp
Аннотация
Введение. Одна из причин наблюдаемого роста заболеваемости злокачественными новообразованиями – отсутствие контроля распространения негенотоксичных канцерогенов.
Цель представленного обзора – анализ проблем в тестировании негенотоксичных канцерогенов и путей создания адекватных подходов к их выявлению посредством анализа эпигенетической активности соединений.
Материал и методы. Проведён анализ более 200 научных публикаций по теме выявления канцерогенной опасности. Использованы базы данных PubMed (149), Scopus (62), Web of Science (33), ResearchGate (15), РИНЦ (12). На основе анализа отобраны 50 наиболее информативных публикаций, отражающих основные аспекты проблемы тестирования негенотоксичных канцерогенов.
Результаты. В статье представлены проблема профилактики канцерогенеза, вызванного негенотоксическими соединениями, актуальность и научное обоснование необходимости тестирования этих соединений, обсуждены существующие подходы к разработке регламентированных мер контроля негенотоксических канцерогенов. Предложен авторский метод выявления эпигенетически активных соединений с помощью генно-модифицированных клеточных систем с репортёрным эпигенетически подавленным геном белка флуорофора в качестве интегрального скринингового теста на потенциальное влияние соединения на систему эпигенетической регуляции экспрессии генов.
Ограничения исследования. Исследование основано на анализе открытых данных по тестированию генотоксических и негенотоксических соединений в вышеупомянутых базах данных.
Заключение. Системно представлены данные, подтверждающие актуальность и необходимость тестирования негенотоксичных канцерогенов, существующие проблемы и способы решения задач в данной области профилактики заболеваемости злокачественными новообразованиями.
Соблюдение этических стандартов. Заключения комиссии по биоэтике не требуется.
Участие авторов:
Якубовская М.Г. – концепция и дизайн исследования, написание текста, редактирование, утверждение окончательного варианта статьи, ответственность за целостность всех частей статьи;
Максимова В.П. – сбор и обработка материала, написание текста по тестированию эпигенетически активных соединений, редактирование;
Белицкий Г.А. – написание текста, редактирование, утверждение окончательного варианта статьи;
Кирсанов К.И. – концепция и дизайн исследования, редактирование, утверждение окончательного варианта статьи, ответственность за целостность всех частей статьи.
Конфликт интересов. Авторы заявляют об отсутствии явных и потенциальных конфликтов интересов в связи с публикацией данной статьи.
Финансирование. Исследование выполнено при поддержке Российского научного фонда, грант №25-15-00432.
Поступила в редакцию: 24 декабря 2025 / Поступила после исправления:12 января 2026 / Принята в печать: 02 февраля 2026 / Опубликована: 18 марта 2026
Ключевые слова
Для цитирования:
Якубовская М.Г., Максимова В.П., Белицкий Г.А., Кирсанов К.И. Проблемы выявления эпигенетически активных негенотоксичных канцерогенов. Токсикологический вестник. 2026;34(1):27-36. https://doi.org/10.47470/0869-7922-2026-34-1-27-36. EDN: ikmcpp
For citation:
Yakubovskaya M.G., Maksimova V.P., Belitsky G.A., Kirsanov K.I. Challenges in the detection of epigenetically active non-genotoxic carcinogens. Toxicological Review. 2026;34(1):27-36. (In Russ.) https://doi.org/10.47470/0869-7922-2026-34-1-27-36. EDN: ikmcpp
Актуальность выявления канцерогенной опасности
Злокачественные новообразования (ЗНО) относятся к числу социально значимых болезней¹. Онкологическая смертность населения занимает второе место после смертности от болезней системы кровообращения (13,8% умерших) [1]. При этом наблюдается рост онкологической заболеваемости в России. Если в 2014 г. на 100 тыс. населения приходилось 2252,4 тыс. онкопациентов, то в 2024 г. этот показатель увеличился до 2948,6, то есть рост за 10 лет составил 30,9% [1]. Основной компонент роста данного показателя – не увеличение продолжительности жизни онкопациента, поскольку согласно целевым показателям федерального проекта «Борьба с онкологическими заболеваниями» за счёт доступности диагностики и лечения злокачественных новообразований увеличение числа пациентов с ЗНО, живущих более пяти лет, должно увеличиться за 2024–2030 гг. лишь на 7%². Динамика роста заболеваемости ЗНО в России соответствует глобальным данным, фиксируемым Всемирной организацией здравоохранения (ВОЗ), и показателям большинства стран. По прогнозам ВОЗ, заболеваемость ЗНО за последующие 20 лет увеличится на 52%. Таким образом, если число заболевших в 2020 г. составляло 19,2 млн человек, то к 2040 г. оно превысит 30,2 млн человек³. В то же время понимание молекулярных механизмов патогенеза ЗНО, накопленная информация об этиологических факторах канцерогенеза, а также эпидемиологические данные, учитывающие экспозицию отдельных групп людей к известным канцерогенным агентам, позволили учёным провести метаанализ влияния факторов окружающей среды на заболеваемость ЗНО и заключить, что реализация мер первичной и вторичной профилактики должна привести к снижению смертности от ЗНО на 70% даже без развития новых подходов к диагностике и лечению [2]. В указанной публикации отмечено также следующее:
- Общество не осознает важности дорогостоящих исследований в области профилактики рака, которые преимущественно являются «убыточными», и их реализации.
- Результат мероприятий по профилактике ЗНО невозможно оценить на коротком интервале времени, он становится очевидным лишь по прошествии многих лет (до 30). Следовательно, быстрая оценка результативности мероприятий невозможна, и целевые показатели могут быть установлены лишь по объёму проведённой работы, а не по достигнутым в течение короткого времени результатам, что делает их менее очевидными для органов государственной власти.
- Исследования по профилактике рака более сложны и объёмны, они требуют анализа на выборках десятков тысяч людей, в то время как для демонстрации совершенствования методов лечения достаточно ≈ 100 онкопациентов.
- Фармацевтические фирмы заинтересованы в развитии и внедрении новых методов лечения, которые более прибыльны по сравнению с внедрением новых методов профилактики.
В результате финансирование исследований, направленных на поиск путей профилактики рака, в разных странах составляет от 2 до 9% от финансирования всех исследований в области онкологии [2]. В силу вышеупомянутых причин ведущую роль в организации профилактических мероприятий должны брать на себя государственные органы, ответственные за качество жизни населения. В частности, эта работа должна проводиться существующими во многих странах национальными комиссиями по канцерогенным факторам.
Комиссия по канцерогенным факторам окружающей среды в СССР и России
В СССР исследования по химическому канцерогенезу и первичной профилактике рака возглавлял академик Л.М. Шабад, инициатор создания Комиссии по канцерогенным веществам и мерам профилактики при Государственной санитарной инспекции Минздрава СССР⁴ [3]. Со дня образования в 1957 г. и до 2020 г. Комиссия была работающим на общественных началах специализированным научно-общественным органом при государственной санитарно-эпидемиологической службе страны (в разное время – при Государственной санитарной инспекции, Главном санэпидуправлении Минздрава СССР, Минздраве СССР, Госкомсанэпиднадзоре России, Минздраве России, Роспотребнадзоре). Следует отметить, что за рубежом аналогичные организации были созданы значительно позже. Так, Международное агентство по изучению рака (International Agency for Research on Cancer, IARC) было учреждено ВОЗ в 1965 г., Национальная токсикологическая программа США (NTP) – в 1972 г., Комитет по канцерогенам Великобритании (CoC) – в конце 1980-х гг. Деятельность Л.М. Шабада в области профилактики рака была отмечена Организацией Объединённых Наций наряду с достижениями таких известных учёных-онкологов, как П. Раус, Л. Гросс, Р. Долл, А. Лакассань и др.⁵.
К 2020 г. Комиссия по канцерогенным веществам и мерам профилактики разработала 7 нормативных документов федерального уровня, которые были введены в действие. Они определяли канцерогенную опасность химических, физических, биологических факторов и производственных процессов для человека, а также основные профилактические мероприятия. В частности, Комиссия разработала документ «Канцерогенные факторы и основные требования к профилактике канцерогенной опасности» (с дополнениями, внесёнными в 2011 и в 2014 гг.), который до 2018 г. был базовым в области первичной профилактики рака в нашей стране⁶. Специалисты Комиссии разработали методические рекомендации по скринингу канцерогенных веществ в объектах окружающей среды, оценке канцерогенной активности веществ, в том числе новых лекарственных препаратов, в хронических экспериментах на животных и в краткосрочных экспериментах. [4]. Эти документы были утверждены в установленном порядке. Комиссия выступила инициатором паспортизации канцерогеноопасных производств [5], совместно с Комиссией по проблемам гигиены и токсикологии пестицидов и агрохимикатов Роспотребнадзора участвовала в решении вопроса о регистрации пестицидов, разработала классификацию пестицидов по степени канцерогенной опасности, используемую и в настоящее время⁷. Члены Комиссии инициировали работу по ратификации Россией Конвенции МОТ № 139 «О борьбе с опасностью, вызываемой канцерогенными веществами и агентами в производственных условиях, и мерах профилактики», что и было выполнено в 2014 г. С 2007 г. специалисты Комиссии ведут информационно-образовательный интернет-портал по первичной профилактике рака (https://www.ppr-inf.ru/). В 2020 г. Роспотребнадзор инициировал реорганизацию Комиссии (завершена в 2025 г.) с формированием проблемной комиссии Роспотребнадзора «Канцерогенные, мутагенные, репротоксические факторы воздействия, эндокринные разрушители»⁸. Её деятельность направлена на совершенствование выявления канцерогенной опасности на основе современных эпидемиологических и механистических данных.
Существующие проблемы выявления канцерогеноопасных соединений
В России тестирование канцерогенной опасности химических соединений проводится с использованием тестов на генотоксическую активность по хорошо отработанным протоколам [6]. Эксперименты на животных для выявления канцерогенной активности в настоящее время проводят лишь в особых ситуациях, например, при выявлении потенциального канцерогенного эффекта в экспериментах по оценке хронической токсичности соединения⁹. При этом используют группы животных по 50 особей, и выявление эффекта даже у одного животного соответствует пределу чувствительности метода лишь в 2%, что является весьма существенным ограничением современного экспериментального тестирования [7, 8]. Появление эпидемиологических данных о влиянии агента на частоту ЗНО однозначно рассматривается как бесспорное доказательство его канцерогенной опасности и требует немедленного пересмотра соответствующих законодательных документов для ограничения его использования¹⁰. Кроме того, согласно современной концепции молекулярного патогенеза ЗНО, основы которой были заложены экспериментальными работами И. Беренблюма и других исследователей в 40-е гг. XX в., канцерогенные агенты подразделяются на генотоксические канцерогены, оказывающие инициирующее воздействие в патогенезе ЗНО, и негенотоксические (эпигенетические), оказывающие промотирующее действие на развитие клона трансформированных клеток и формирование опухоли [9–11]. Исследования канцерогенов окружающей среды, обладающих доказанным или вероятным негенотоксичным канцерогенным действием, постоянно расширяются. Становится очевидной необходимость включения в анализ канцерогенной опасности данных о проканцерогенной активности негенотоксичных соединений окружающей среды [12–14]. Эту необходимость иллюстрирует пример трагических последствий применения в медицинской практике диэтилстильбестрола в качестве средства для сохранения беременности. Его канцерогенные свойства проявились спустя годы у детей, в лечении матерей которых применяли этот препарат [15]. Наряду с диэтилстильбестролом к числу негенотоксических веществ с выраженной проканцерогенной активностью относятся многие соединения разных классов, в том числе установленные промоторы канцерогенеза (пентахлорфенол, фенобарбитал, полихлорированные бифенилы, кротоновое масло и др.), эндокринные модификаторы и гормональные дизрапторы (финастеридин, винклозин, амитрол, сульфаметазин, эстрогены, модификаторы атразина, ингибиторы допамина и др.), многочисленные цитотоксины (арохлор, бутахлор, четыреххлористый углерод, фталаты и др.), мелкодисперсные частицы, металлы (кадмий, никель, свинец, ртуть и др.) [7, 11]. Недавно опубликованы данные о повышении риска развития рака молочной железы при кумулятивной экспозиции к пестицидам, диоксинам, растворителям и другим соединениям, загрязняющим окружающую среду [16]. Показана ассоциация загрязнения атмосферного воздуха негенотоксичными выхлопами автотранспорта с нарушениями, вовлечёнными в патогенез рака молочной железы [17]. Накопленная за последние 30 лет информация о биологии опухолевой клетки, эпигенетической регуляции экспрессии генов, а также о механизмах действия негенотоксичных канцерогенов открывает новые возможности организации скрининга негенотоксичных канцерогенов, с неконтролируемым распространением которых связывают неуклонное повышение заболеваемости ЗНО [7, 13, 18]. Для решения этой задачи Международное агентство по изучению рака (IARC – англ. International Agency for Research on Cancer) разработало новый подход к определению канцерогенной опасности на основе оценки ключевых характеристик канцерогенных соединений, к которым были отнесены следующие [19]:
- электрофильность или способность превращаться в электрофилы;
- генотоксичность;
- способность индуцировать оксидативный стресс;
- способность влиять на эпигенетическую регуляцию экспрессии генов (эпигенетическая проканцерогенная активность);
- способность влиять на репарацию ДНК;
- способность индуцировать хроническое воспаление;
- иммуносупрессорные свойства;
- способность влиять на рецепторы клетки, активирующие проканцерогенный клеточный сигналинг;
- способность вызывать иммортализацию клеток;
- способность активировать пролиферацию и ингибировать программируемую клеточную гибель.
Следует отметить, что лишь три первые из перечисленных десяти характеристик канцерогенных соединений обусловливают прямую инициацию канцерогенеза, а остальные соответствуют их способности быть регуляторами отдельных жизненно важных для клетки или организма процессов. У многих генотоксичных канцерогенов была обнаружена способность вызывать проканцерогенный негенотоксический эффект [19]. Негенотоксические эффекты можно выявлять по механистическим данным, полученным in vitro, в том числе, по митогенной активности, изменениям клеточного сигналинга, подавлению ответа клетки на повреждение ДНК (DNA damage respionce, DDR), подавлению апоптоза и др. На совместном заседании (2018 г.) с участием более 100 специалистов-экспертов в области химического канцерогенеза IARC официально приняло изменения процедуры установления канцерогенной опасности различных агентов на основании учёта механистических данных [19]. В связи с этим страны Организации экономического сотрудничества и развития (OECD) в 2020 г. сформировали международный научный комитет по подготовке рабочего плана создания унифицированных методических подходов к скринингу негенотоксичных канцерогенов [18]. Актуальность этих действий определили следующие обстоятельства: (1) масштаб воздействия – широкие массы населения, которое может подвергнуться возможному канцерогенному воздействию; (2) тяжесть последствий – онкологическая заболеваемость, смертность и инвалидность; (3) неизбежный путь поступления (атмосферный воздух, питьевая вода); (4) вероятность отдалённых неблагоприятных эффектов на протяжении всей жизни человека; (5) уязвимость таких групп населения, как дети, инвалиды, пожилые люди; (6) потенциальная возможность предотвращения воздействия; (7) необходимость идентификации рисков, связанных с использованием новых соединений (агентов ). На основе анализа более 700 научных публикаций, посвящённых механизмам действия негенотоксичных соединений, и детального обсуждения более 200 опубликованных методических подходов к выявлению активации этих механизмов, были сформированы шесть групп тестов, выявляющих: (1) индукторы воспаления; (2) иммуномодуляторы; (3) агенты, повреждающие клеточные структуры; (4) митогенные соединения; (5) индукторы гиперплазии; (6) индукторы дисплазии (рисунок).
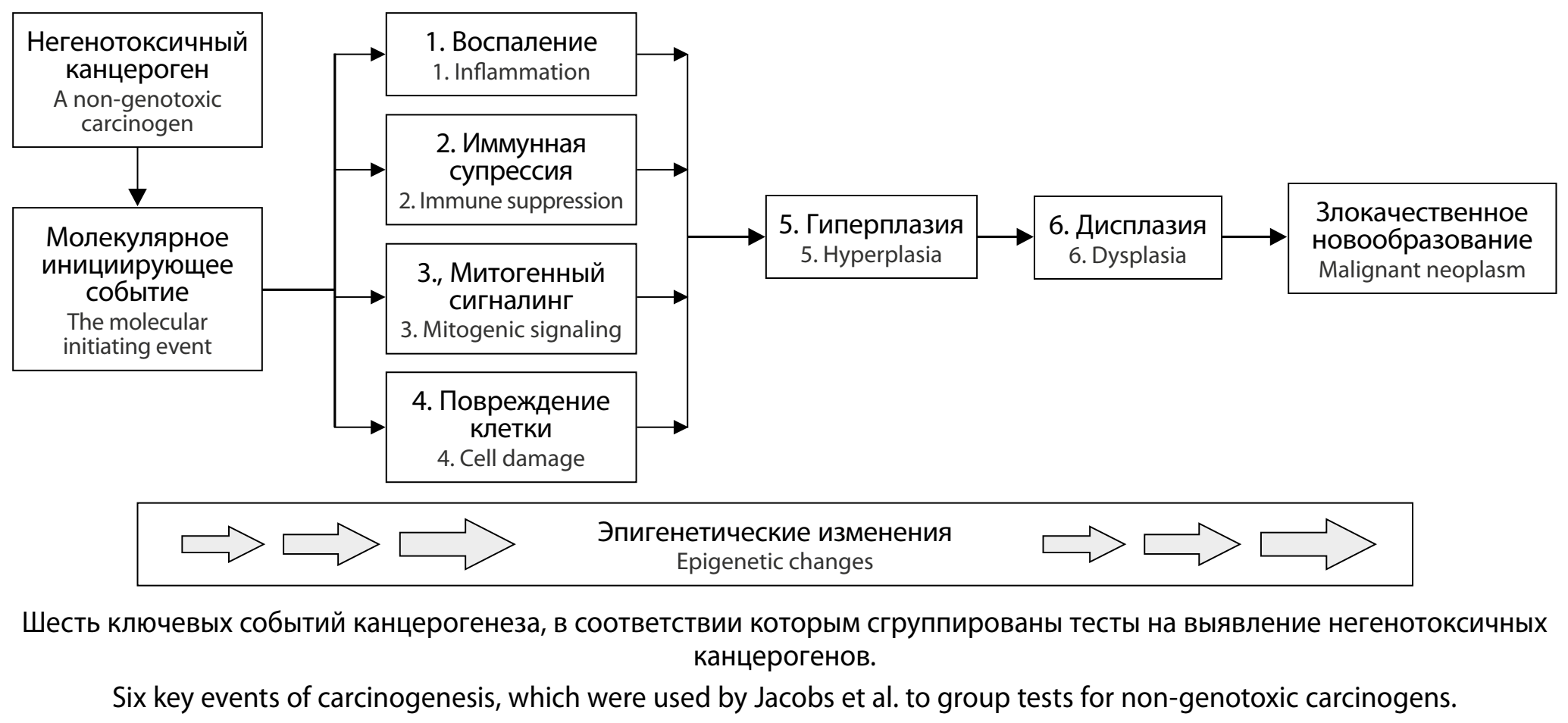
При этом было отмечено, что все используемые тесты должны сопровождаться анализом влияния изучаемых соединений на систему эпигенетической регуляции экспрессии генов как систему, определяющую функционирование генома, согласно основной молекулярно-биологической догме «ДНК → РНК → Белок» как в нормальной, так и в опухолевой клетке [7, 18, 20].
Эпигенетическая регуляция экспрессии генов и канцерогенез
Исследования механизмов эпигенетической регуляции экспрессии генов, начатые Н.К. Кольцовым в первой половине XX века, получили бурное развитие в середине 1990-х гг. [21]. В настоящее время очевидно, что эпигенетическое замалчивание генов является важным механизмом регуляции функционирования генома и включает метилирование ДНК, модификации гистонов, интерференцию нкРНК и ремоделирование хроматина [22, 23]. Эпигенетическая регуляция экспрессии генов участвует в процессах транспозиции мобильных элементов, геномном импринтинге, контроле клеточного цикла и тканевой дифференцировки [24–27]. Благодаря эпигенетической регуляции также происходит адаптация организма и отдельных клеток к изменениям окружающей среды и микроокружения соответственно [28, 29]. Экзогенные факторы, влияющие на эпигенетическую регуляцию, могут как вызывать адаптивные изменения, так и нарушать ключевые клеточные процессы, приводя к ЗНО и другим патологиям [30–32]. Биомониторинговые популяционные исследования выявили неблагоприятное воздействие многих широко распространённых эпигенетически активных веществ: ряда фармакологических препаратов, пищевых добавок и загрязнений окружающей среды [33–35].
В настоящее время человечество использует более 90 000 химических веществ, а эпигенетическая активность была оценена только для небольшой их части (< 2%) [36]. Ситуация осложняется непрерывным появлением новых соединений и ростом годового оборота уже используемых в быту и на производствах химических соединений, который за последние десять лет удвоился [36, 37]. Следовательно, необходим скрининг ксенобиотиков на эпигенетическую активность до начала их широкого применения. Это позволит избежать воздействия потенциально опасных соединений на всё население или отдельные группы и выбрать более безопасные соединения с полезными потребительскими свойствами. Применение методов молекулярной биологии в экологической эпидемиологии, наряду с их несомненным научным вкладом в изучение механизмов канцерогенеза, может существенно сократить временные и финансовые затраты при выявлении экологических факторов онкологического риска.
Существование методов скрининга, обладающих высокой производительностью, дающих чёткие критерии активности и низкий уровень ложноположительных и ложноотрицательных результатов, а также позволяющих проведение широких скрининговых мероприятий, является критическим для тестирования химических соединений на эпигенетическую активность. Одной из первых работ, обосновавших необходимость создания тест-систем для скрининга ксенобиотиков на эпигенетическую активность, была публикация по негенотоксическим эффектам химических соединений сотрудников IARC в 2013 г. [38]. К настоящему времени для изучения эпигенетических эффектов ксенобиотиков разработаны различные модельные системы in vivo и in vitro [23]. Большой вклад в изучение эпигенетических эффектов загрязнений окружающей среды был сделан учёными, использовавшими в экспериментах Drosophila, Arabidopsis, Daphnia и Xenopus laevis [39]. Тест-системы in vivo включают и мышиные модели, в которых эпигенетическое влияние отражают изменения окраски шерсти и морфологии хвоста. В частности, мыши Avy служат очень хорошими эпигенетическими биосенсорами in vivo для оценки влияния ксенобиотиков на систему эпигенетической регуляции транскрипции [40]. Однако использование этих организмов ограничено видовыми функциональными особенностями системы эпигенетической регуляции мышей, и такие исследования относятся к весьма трудозатратным и дорогостоящим. Кроме того, традиционные тесты на животных вызывают серьёзные этические проблемы [8, 23]. Наиболее удобные методы скрининга эпигенетически активных соединений основаны на модельных системах in vitro с использованием опухолевых и условно нормальных иммортализованных клеток человека [20, 36, 41]. Преимущества таких клеточных технологий заключаются в низкой себестоимости и краткосрочности тестирования. Тест-системы in vitro были разработаны для выявления глобальных изменений метилирования и изменений сайт-специфического метилирования ДНК [42, 43]. Однако первые тест-системы недостаточно чувствительны для выявления различных специфических для сайта изменений, а последние не позволяют оценивать глобальные эффекты. На основе технологии геномного редактирования CRISPR/Cas9/Cas12a был предложен новый тест, выявляющий множественные «конечные точки» и характеризующийся высокой пропускной способностью, однако эти системы ограничены набором ферментов, которые могут быть подвергнуты генетическому редактированию [44, 45]. Martinez E.D. et al. описали разработку флуоресцентного репортёрного анализа на реактивацию эпигенетически подавленных генов с выявлением разных механизмов действия эпигенетически активных соединений [46]. При создании данной тест-системы клетки аденокарциномы молочной железы мыши C127 трансфицировали вектором, содержащим репортёрный флуоресцентный белок GFP под промотором CMV, и аминогликозидфосфотрансферазу, обеспечивающую резистентность к неомицину. Клетки, устойчивые к неомицину, с эпигенетически подавленной экспрессией GFP было предложено использовать в качестве тест-системы на эпигенетическую активность. Авторы описанной тест-системы использовали всего три известных ингибитора эпигенетического замалчивания в качестве положительного контроля (трихостатин A, бутират натрия и 5-азацитидин), а спектр выявляемых эпигенетических эффектов в полученной тест-системе проанализирован не был. Тем не менее было продемонстрировано, что тест-система на основе клеток мыши C127, в отличие от других описанных выше методов обнаружения эпигенетических эффектов, позволяла одновременно выявлять ингибиторы гистоновых деацетилаз и метилтрансфераз.
В 2010 г. группа американских вирусологов опубликовала результаты исследования, посвящённого моделированию в единой системе 15 различных механизмов эпигенетического подавления экспрессии вирусного генома, интегрированного в геном клеток HeLa [47]. При получении данной модельной системы были использованы клетки HeLa, инфицированные лентивирусным вектором, содержащим репортёрный ген GFP, а затем был проведён трёхкратный клеточный сортинг вариантов клеток, содержащих эпигенетически репрессированный ген GFP (рис. 3) [48]. Эта популяция клеток получила название HeLa TI. Мы предположили, что при воздействии на клетки HeLa TI ксенобиотиков, способных влиять на систему эпигенетической регуляции, должна происходить активация экспрессии GFP, которая может быть оценена с помощью проточной цитометрии. В исследовании В.П. Максимовой и соавт. были продемонстрирована эффекты 15 известных ингибиторов ферментов эпигенетической регуляции, что свидетельствовало о пригодности HeLa TI для проведения скрининговых анализов на эпигенетическую активность химических соединений [49]. Таким образом, к настоящему времени продемонстрирована перспективность использования для скрининга химических соединений на эпигенетическую активность генно-модифицированных клеточных популяций, полученных с помощью клеточного сортинга, позволившего отобрать клетки с эпигенетически репрессированным репортёрным геном белка-флуорофора. Разработанная тест-система основана на использовании репортёрного анализа, что обеспечивает её высокую пропускную способность при применении в скрининговых целях, относительно невысокую стоимость и быстроту анализа, а также простоту в интерпретации результатов. Следует учитывать, что изменение эпигенетической регуляции может иметь различную направленность, то есть обладать как проканцерогенным, так и антиканцерогенным эффектом, и для выявления эпигенетических канцерогенов и антиканцерогенов необходим последующий транскриптомный анализ. Однако выявление эпигенетически активных соединений существенно сократит объёмы более дорогостоящих и трудоёмких транскриптомных исследований с помощью системы генно-модифицированных клеток с эпигенетически подавленным репортёрным флуорофором, что позволит ускорить и удешевить выявление канцерогеноопасных эпигенетически активных соединений [49, 50].
В то же время тест-система, представленная генно-модифицированными клетками HeLa TI, имеет ряд ограничений. К ним следует отнести следующие: (1) клетки HeLa инфицированы вирусом HPV18, что определило низкий уровень метилирования, не позволяющий использовать эти клетки для последующего анализа глобальных эффектов ксенобиотиков по снятию метилирования; (2) эпигенетический ландшафт клеток, использованных при получении тесторной популяции, должен влиять на результаты тестирования, и для получения более объективной информации об эпигенетических эффектах соединений необходимо использовать клетки различного гистогенеза; (3) со времени получения популяции клеток HeLa TI c репортёрным трансгеном GFP, экспрессия которого подавлена с помощью одного из 15 механизмов эпигенетической регуляции экспрессии генов, прошло почти 20 лет, и в настоящее время использованный флуорофор и метод его доставки в клетку не являются оптимальными. Полученные данные и анализ недостатков данной скрининговой системы позволяют подойти к созданию более совершенных систем для выявления эпигенетически активных соединений с использованием генно-модифицированных клеток с репортёрным геном флуорофора, что свидетельствует о перспективности данного подхода к выявлению негенотоксичных канцерогенов.
Заключение
Согласно современной концепции канцерогенеза, наиболее распространёнными этиологическими факторами злокачественных новообразований (ЗНО) являются химические агенты. Развитие методов скрининга соединений, способных вызывать повреждения ДНК и приводить к генным и геномным нарушениям, то есть генотоксических канцерогенов, позволили предотвратить или значительно снизить экспозицию людей к таким агентам. О результативности данного подхода свидетельствует снижение частоты профессиональных ЗНО и заболеваемости раком лёгких в результате сокращения табакокурения. Тем не менее онкологическая заболеваемость продолжает расти, и международное научное сообщество рассматривает в качестве одной из причин этого роста отсутствие контроля негенотоксических канцерогенов, которые могут многократно усиливать действие генотоксичных агентов, оказывая промотирующее действие на формирование опухоли. Негенотоксичные канцерогены были впервые описаны более 80 лет назад, однако подходы к их скринингу до сих пор не сформированы. Это связано с большим разнообразием механизмов действия негенотоксичных канцерогенов и отсутствием чётких критериев тестирования. При этом анализ всех возможных эффектов соединения является трудоёмким и дорогостоящим. Реализация действия негенотоксичных канцерогенов, как отмечено во многих научных публикациях, происходит путём активации эпигенетических механизмов регуляции транскрипции, однако существующие модельные системы направлены на оценку отдельных эпигенетических эффектов ксенобиотиков. Современной попыткой создания системы скрининга негенотоксичных канцерогенов стал проект международной рабочей группы Организации экономического сотрудничества и развития. Согласно этому проекту, более 200 методов скрининга негенотоксичных канцерогенов объединены в шесть блоков. При этом отмечена необходимость тестирования соединений на эпигенетическую активность.
В отделе химического канцерогенеза ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России был выполнен ряд исследований, посвящённых апробации в качестве тест-системы на выявление эпигенетически активных соединений популяции клеток HeLa TI, имеющих в своём геноме эпигенетически репрессированный репортёрный ген белка-флуорофора GFP. Результаты исследования свидетельствуют о перспективности использования для скрининга эпигенетически активных соединений генно-модифицированных клеточных популяций, полученных с помощью сортинга клеток, на присутствие в них эпигенетически репрессированного репортёрного гена белка-флуорофора. Таким образом, сформирован принципиально новый подход к обнаружению проявляющих свой эффект по эпигенетическим механизмам канцерогенов, не выявляемых принятыми в настоящее время тестами на генотоксичность. Поиск путей контроля негенотоксичных канцерогенов продолжает оставаться актуальной задачей, стоящей перед специалистами проблемной комиссии Роспотребнадзора «Канцерогенные, мутагенные, репротоксические факторы воздействия, эндокринные разрушители».
¹ Постановление Правительства Российской Федерации от 1 декабря 2004 N 715.
² Структура и ключевые мероприятия федерального проекта «Борьба с онкологическими заболеваниями» 08.08.2025 https://minzdrav.gov.ru/poleznye-resursy/natsionalnye-proekty-rossii-prodolzhitelnaya-i-aktivnaya-zhizn-novye-tehnologii-sberezheniya-zdorovya/struktura-i-klyuchevye-meropriyatiya-federalnogo-proekta-borba-s-onkologicheskimi-zabolevaniyami (дата обращения 16.01.2026).
³ International Agency for Research Cancer: CANCER TOMORROW. URL: https://gco.iarc.fr/tomorrow/en (дата обращения 07.11.2022).
⁴ Приказ по Министерству здравоохранения СССР № 103 от 15 марта 1957 г. «О назначении Комиссии по канцерогенным веществам и мерам профилактики при Государственной санитарной инспекции Министерства здравоохранения СССР».
⁵ Резолюция генеральной ассамблеи ООН 1398 (XIV) от 10.10.1962. URL: https://www.un.org/sites/un2.un.org/files/webform/a17-special_sess-4_0_0_0.pdf
⁶ СанПиН 1.2.2353–08 (с дополнениями, внесёнными в 2011 и в 2014 гг.) «Канцерогенные факторы и основные требования к профилактике канцерогенной опасности»
⁷ Санитарные правила и нормативы. СанПиН 1.2.2584–10 «Гигиенические требования к безопасности процессов испытаний, хранения, перевозки, реализации, применения, обезвреживания и утилизации пестицидов и агрохимикатов».
⁸ Приказ Роспотребнадзора от 22.09.2025 № 660. Об утверждении составов проблемных комиссий Учёного совета Роспотребнадзора. Приложение 18 «Состав проблемной комиссии Учёного совета Роспотребнадзора «Федеральный проект «Канцерогенные, мутагенные, репротоксические факторы воздействия, эндокринные разрушители».
⁹ Метод ОЭСР № 453 «Комбинированные исследования хронической токсичности и канцерогенности» (англ. OECD Test Guideline No. 453 "Combined Chronic Toxicity/ Carcinogenicity Studies").
¹⁰ IARC Monographs Preamble – Preamble to the IARC Monographs on the Identification of Carcinogenic Hazards to Humans (amended January 2019). URL: https://monographs.iarc.who.int/wp-content/uploads/2019/07/Preamble-2019.pdf
Список литературы
1. Каприн А.Д., Старинский В.В., Шахзадова А.О. Злокачественные новообразования в России в 2019 году (заболеваемость и смертность). М.; 2020.
2. Song M., Vogelstein B., Giovannucci E.L., Willett W.C., Tomasetti C. Cancer prevention: Molecular and epidemiologic consensus. Science. 2018; 361(6409): 1317–8. https://doi.org/10.1126/science.aau3830
3. Ильницкий А.П. 60 лет деятельности комиссии по канцерогенным факторам. Здравоохранение Российской Федерации. 2018; 62(3): 157–63. https://doi.org/10.18821/0044-197X-2018-62-3-157-163 https://elibrary.ru/uxqgth
4. Хабриев Р.У. Руководство по экспериментальному (доклиническому) изучению новых фармакологических веществ. М.: Медицина; 2005. https://elibrary.ru/qciiob
5. Организация и проведение санитарно-гигиенической паспортизации канцерогеноопасных производств. Методические указания. М.; 1998.
6. Хамидулина Х.Х., Тарасова Е.В., Назаренко А.К., Тверская А.С., Дорофеева Е.В., Замкова И.В. и др. Особенности формирования доказательной базы при оценке и классификации опасности химических веществ по специфическим и отдалённым эффектам. Токсикологический вестник. 2025; 33(6): 502–12.
7. Белицкий Г.А., Кирсанов К.И., Лесовая Е.А., Максимова В.П., Соленова Л.Г., Якубовская М.Г. Химический канцерогенез и первичная профилактика рака. М.: АБВ-пресс; 2020.
8. Suarez-Torres J.D., Orozco C.A., Ciangherotti C.E. The 2-year rodent bioassay in drug and chemical carcinogenicity testing: Performance, utility, and configuration for cancer hazard identification. J. Pharmacol. Toxicol. Methods. 2021; 110: 107070. https://doi.org/10.1016/j.vascn.2021.107070
9. Berenblum I. The cocarcinogenic action of croton resin. Cancer Res. 1941; 1: 44–50.
10. Berenblum I. Cancer prevention as a realizable goal. Cancer. 1981; 47(10): 2346–8. https://doi.org/10.1002/1097-0142(19810515)47:10%3C2346::aid-cncr2820471004%3E3.0.co;2-x
11. Kobets T., Iatropoulos M.J., Williams G.M. Mechanisms of DNA-reactive and epigenetic chemical carcinogens: applications to carcinogenicity testing and risk assessment. Toxicol. Res. (Camb.). 2019; 8(2): 123–45. https://doi.org/10.1039/c8tx00250a
12. Шалгинских Н.А., Карпеченко Н.Ю., Оглоблина А.М., Лесовая Е.А., Кирсанов К.И., Набережнов Д.С., и др. Эпигенетические механизмы регуляции экспрессии генов в химическом канцерогенезе. Вопросы биологической, медицинской и фармацевтической химии. 2014; (3): 46–64. https://elibrary.ru/rydikr
13. Ревазова Ю.А., Илюшина Н.А. К вопросу о негенотоксических канцерогенах. Токсикологический вестник. 2021; 29(4): 51–5. https://doi.org/10.36946/0869-7922-2021-29-4-51-55 https://elibrary.ru/hgulew
14. Desaulniers D., Vasseur P., Jacobs A., Aguila M.C., Ertych N., Jacobs M.N. Integration of epigenetic mechanisms into non-genotoxic carcinogenicity hazard assessment: focus on DNA methylation and histone modifications. Int. J. Mol. Sci. 2021; 22(20): 10969. https://doi.org/10.3390/ijms222010969
15. Veurink M., Koster M., Berg L.T. The history of DES, lessons to be learned. Pharm. World Sci. 2005; 27(3): 139–43. https://doi.org/10.1007/s11096-005-3663-z
16. Rodgers K.M., Udesky J.O., Rudel R.A., Brody J.G. Environmental chemicals and breast cancer: An updated review of epidemiological literature informed by biological mechanisms. Environ. Res. 2018; 160: 152–82. https://doi.org/10.1016/j.envres.2017.08.045
17. Sahay D., Terry M.B., Miller R. Is breast cancer a result of epigenetic responses to traffic-related air pollution? A review of the latest evidence. Epigenomics. 2019; 11(6): 701–14. https://doi.org/10.2217/epi-2018-0158
18. Jacobs M.N., Colacci A., Corvi R., Vaccari M., Aguila M.C., Corvaro M., et al. Chemical carcinogen safety testing: OECD expert group international consensus on the development of an integrated approach for the testing and assessment of chemical non-genotoxic carcinogens. Arch. Toxicol. 2020; 94(8): 2899–23. https://doi.org/10.1007/s00204-020-02784-5
19. Samet J.M., Chiu W.A., Cogliano V., Jinot J., Kriebel D., Lunn R.M., et al. The IARC monographs: updated procedures for modern and transparent evidence synthesis in cancer hazard identification. J. Natl Cancer Inst. 2020; 112(1): 30–7. https://doi.org/10.1093/jnci/djz169
20. Goodman S., Chappell G., Guyton K.Z., Pogribny I.P., Rusyn I. Epigenetic alterations induced by genotoxic occupational and environmental human chemical carcinogens: An update of a systematic literature review. Mutat. Res. Rev. Mutat. Res. 2022; 789: 108408. https://doi.org/10.1016/j.mrrev.2021.108408
21. Koltzoff N.K. Physiologie du de’velopment et genetique. Actualites scientifiques et Industrielles. Paris: Hermann et C-ie; 1935. (in French)
22. Allis C.D., Jenuwein T. The molecular hallmarks of epigenetic control. Nat. Rev. Genet. 2016; 17(8): 487–500. https://doi.org/10.1038/nrg.2016.59
23. Максимова В.П., Усалка О.Г., Макусь Ю.В., Попова В.Г., Трапезникова Е.С., Хайриева Г.И., и др. Нарушение метилирования ДНК при злокачественных новообразованиях. Успехи молекулярной онкологии. 2022; 9(4): 24–40. https://doi.org/10.17650/2313-805X-2022-9-4-24-40 https://elibrary.ru/scidnm
24. Slotkin R.K., Martienssen R. Transposable elements and the epigenetic regulation of the genome. Nat. Rev. Genet. 2007; 8(4): 272–85. https://doi.org/10.1038/nrg2072
25. Misiak B., Ricceri L., Sasiadek M.M. Transposable elements and their epigenetic regulation in mental disorders: current evidence in the field. Front. Genet. 2019; 10: 580. https://doi.org/10.3389/fgene.2019.00580
26. Prins G.S. Estrogen imprinting: when your epigenetic memories come back to haunt you. Endocrinology. 2008; 149(12): 5919–21. https://doi.org/10.1210/en.2008-1266
27. Stewart-Morgan K.R., Petryk N., Groth A. Chromatin replication and epigenetic cell memory. Nat. Cell Biol. 2020; 22(4): 361–71. https://doi.org/10.1038/s41556-020-0487-y
28. Perera B.P.U., Svoboda L., Dolinoy D.C. Genomic tools for environmental epigenetics and implications for public health. Curr. Opin. Toxicol. 2019; 18: 27–33. https://doi.org/10.1016/j.cotox.2019.02.008
29. Cavalli G., Heard E. Advances in epigenetics link genetics to the environment and disease. Nature. 2019; 571(7766): 489–99. https://doi.org/10.1038/s41586-019-1411-0
30. Chung F.F., Herceg Z. The promises and challenges of toxico-epigenomics: environmental chemicals and their impacts on the epigenome. Environ. Health Perspect. 2020; 128(1): 15001. https://doi.org/10.1289/ehp6104
31. Marczylo E.L., Jacobs M.N., Gant T.W. Environmentally induced epigenetic toxicity: potential public health concerns. Crit. Rev. Toxicol. 2016; 46(8): 676–700. https://doi.org/10.1080/10408444.2016.1175417
32. Bijlsma N., Cohen M.M. Environmental chemical assessment in clinical practice: unveiling the elephant in the room. Int. J. Environ. Res. Public Health. 2016; 13(2): 181. https://doi.org/10.3390/ijerph13020181
33. Wang T., Pehrsson E.C., Purushotham D., Li D., Zhuo X., Zhang B., et al. The NIEHS TaRGET II Consortium and environmental epigenomics. Nat. Biotechnol. 2018; 36(3): 225–7. https://doi.org/10.1038/nbt.4099
34. Moreno F.S., Heidor R., Pogribny I.P. Nutritional epigenetics and the prevention of hepatocellular carcinoma with bioactive food constituents. Nutr. Cancer. 2016; 68(5): 719–33. https://doi.org/10.1080/01635581.2016.1180410
35. Angrish M.M., Allard P., McCullough S.D., Druwe I.L., Chadwick L., Hines E., et al. Epigenetic applications in adverse outcome pathways and environmental risk evaluation. Environ. Health Perspect. 2018; 126(4): 045001. https://doi.org/10.1289/ehp2322
36. Cote I.L., McCullough S.D., Hines R.N., Vandenberg J.J. Application of epigenetic data in human health risk assessment. Curr. Opin. Toxicol. 2017; 6: 71–8. https://doi.org/10.1016/j.cotox.2017.09.002
37. Chen Z., Liu Y., Wright F.A., Chiu W.A., Rusyn I. Rapid hazard characterization of environmental chemicals using a compendium of human cell lines from different organs. ALTEX. 2020; 37(4): 623–38. https://doi.org/10.14573/altex.2002291
38. Herceg Z., Lambert M.P., van Veldhoven K., Demetriou C., Vineis P., Smith M.T., et al. Towards incorporating epigenetic mechanisms into carcinogen identification and evaluation. Carcinogenesis. 2013; 34(9): 1955–67. https://doi.org/10.1093/carcin/bgt212
39. Bonasio R. The expanding epigenetic landscape of non-model organisms. J. Exp. Biol. 2015; 218(Pt. 1): 114–22. https://doi.org/10.1242/jeb.110809
40. Dolinoy D.C. The agouti mouse model: an epigenetic biosensor for nutritional and environmental alterations on the fetal epigenome. Nutr. Rev. 2008; 66(Suppl. l): S7–11. https://doi.org/10.1111/j.1753-4887.2008.00056.x
41. Parfett C.L., Desaulniers D. A Tox21 approach to altered epigenetic landscapes: assessing epigenetic toxicity pathways leading to altered gene expression and oncogenic transformation in vitro. Int. J. Mol. Sci. 2017; 18(6): 1179. https://doi.org/10.3390/ijms18061179
42. Yoshida W., Baba Y., Karube I. Global DNA methylation detection system using MBD-fused luciferase based on bioluminescence resonance energy transfer assay. Anal. Chem. 2016; 88(18): 9264–8. https://doi.org/10.1021/acs.analchem.6b02565
43. Han W., Shi M., Spivack S.D. Site-specific methylated reporter constructs for functional analysis of DNA methylation. Epigenetics. 2013; 8(11): 1176–87. https://doi.org/10.4161/epi.26195
44. Campa C.C., Weisbach N.R., Santinha A.J., Incarnato D., Platt R.J. Multiplexed genome engineering by Cas12a and CRISPR arrays encoded on single transcripts. Nat. Methods. 2019; 16(9): 887–93. https://doi.org/10.1038/s41592-019-0508-6
45. Ding X., Seebeck T., Feng Y., Jiang Y., Davis G.D., Chen F. Improving CRISPR-Cas9 genome editing efficiency by fusion with chromatin-modulating peptides. CRISPR J. 2019; 2: 51–63. https://doi.org/10.1089/crispr.2018.0036
46. Martinez E.D., Dull A.B., Beutler J.A., Hager G.L. High-content fluorescence‐based screening for epigenetic modulators. Methods Enzymol. 2006; 414: 21–36. https://doi.org/10.1016/s0076-6879(06)14002-1
47. Poleshko A., Einarson M.B., Shalginskikh N., Zhang R., Adams P.D., Skalka A.M., et al. Identification of a functional network of human epigenetic silencing factors. J. Biol. Chem. 2010; 285(1): 422–33. https://doi.org/10.1074/jbc.m109.064667
48. Poleshko A., Palagin I., Zhang R., Boimel P. Identification of cellular proteins that maintain retroviral epigenetic silencing: evidence for an antiviral response. J. Virol. 2008; 82(5): 2313–23. https://doi.org/10.1128/jvi.01882-07
49. Maksimova V., Shalginskikh N., Vlasova O., Usalka O., Beizer A., Bugaeva P., et al. HeLa TI cell-based assay as a new approach to screen for chemicals able to reactivate the expression of epigenetically silenced genes. PloS One. 2021; 16(6): e0252504. https://doi.org/10.1371/journal.pone.0252504
50. Oku Y., Madia F., Lau P., Paparella M., McGovern T., Luijten M., et al. Analyses of transcriptomics cell signalling for pre-screening applications in the integrated approach for testing and assessment of non-genotoxic carcinogens. Int. J. Mol. Sci. 2022; 23(21): 12718. https://doi.org/10.3390/ijms232112718
Об авторах
Марианна Геннадиевна ЯкубовскаяРоссия
Доктор медицинских наук, заведующая отделом молекулярных механизмов канцерогенеза НИИ экспериментальной онкологии и канцерогенеза; профессор кафедры последипломного образования врачей департамента профессионального образования ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России 115522, Москва, Россия; главный научный сотрудник НИИ молекулярной и клеточной медицины МИ ФГАОУ ВО РУДН им. Патриса Лумумбы, 117198, Москва, Россия
e-mail: mgyakubovskaya@mail.ru
Варвара Павловна Максимова
Россия
Младший научный сотрудник лаборатории канцерогенных веществ отдела изучения молекулярных механизмов канцерогенеза НИИ экспериментальной онкологии и канцерогенеза ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России, 115522, Москва, Россия
e-mail: lavarvar@gmail.com
Геннадий Альтерович Белицкий
Россия
Главный научный консультант отдела молекулярных механизмов канцерогенеза НИИ экспериментальной онкологии и канцерогенеза; профессор кафедры последипломного образования врачей департамента профессионального образования ФГБУ «НМИЦ онкологии им. Н.Н. Блохина», 115522, Москва, Россия
e-mail: belitsga@gmail.com
Кирилл Игоревич Кирсанов
Россия
Доктор биологических наук, заведующий лабораторией канцерогенных веществ отделом изучения молекулярных механизмов канцерогенеза НИИ экспериментальной онкологии и канцерогенеза; доцент кафедры последипломного образования врачей департамента профессионального образования ФГБУ «НМИЦ онкологии им. Н.Н. Блохина», 115522, Москва, Россия; профессор кафедры общей врачебной практики Медицинского института ФГАОУ ВО «Российский университета дружбы народов им. Патриса Лумумбы», 117198, Москва, Россия
e-mail: kkirsanov85@yandex.ru
Рецензия
Для цитирования:
Якубовская М.Г., Максимова В.П., Белицкий Г.А., Кирсанов К.И. Проблемы выявления эпигенетически активных негенотоксичных канцерогенов. Токсикологический вестник. 2026;34(1):27-36. https://doi.org/10.47470/0869-7922-2026-34-1-27-36. EDN: ikmcpp
For citation:
Yakubovskaya M.G., Maksimova V.P., Belitsky G.A., Kirsanov K.I. Challenges in the detection of epigenetically active non-genotoxic carcinogens. Toxicological Review. 2026;34(1):27-36. (In Russ.) https://doi.org/10.47470/0869-7922-2026-34-1-27-36. EDN: ikmcpp
JATS XML





































